题目内容
人们发现,用氯化钯(PdCl2)溶液可检验一氧化碳对空气的污染程度.一氧化碳与氯化钯溶液反应,生成了黑色的金属钯(Pd)粉末,反应的化学方程式是:PdCl2+CO+H2O=Pd↓+CO2+2HCl
现将84L空气(密度为1.29g/L)通入足量的氯化钯溶液中,完全反应后生成了0.212g沉淀.求所测空气中一氧化碳的质量分数.(精确到0.001%)(相对原子质量:C-12 O-16 Pd-106)
现将84L空气(密度为1.29g/L)通入足量的氯化钯溶液中,完全反应后生成了0.212g沉淀.求所测空气中一氧化碳的质量分数.(精确到0.001%)(相对原子质量:C-12 O-16 Pd-106)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据反应的化学方程式,可确定反应中钯与一氧化碳的质量关系,利用这一质量关系,由反应后得到Pd的质量可计算反应消耗一氧化碳的质量.
解答:解:设所测空气中一氧化碳的质量分数为x.
PdCl2+CO+H2O=Pd↓+CO2+2HCl
28 106
84L×l.29g/L×x 0.212g
=
x=0.052%
答:所测空气中一氧化碳的质量分数为0.052%.
PdCl2+CO+H2O=Pd↓+CO2+2HCl
28 106
84L×l.29g/L×x 0.212g
| 28 |
| 84L×1.29g/L×x |
| 106 |
| 0.212g |
x=0.052%
答:所测空气中一氧化碳的质量分数为0.052%.
点评:本题为根据化学方程式的基础计算,完整的计算过程、规范的书写格式、正确的计算结果是解答此类问题时需要认真对待的.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
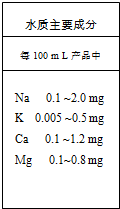 某饮用水标签的部分内容如图所示,这里的K、Ca等是指( )
某饮用水标签的部分内容如图所示,这里的K、Ca等是指( )| A、原子 | B、分子 | C、元素 | D、金属 |
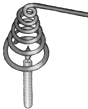 用粗铜丝绕成一个内径比蜡烛直径稍小一点的线圈,圈与圈之间有一定的空隙.点燃蜡烛,把铜丝制成的线圈从火焰上面罩下去,正好把蜡烛的火焰罩在铜丝里面(如图所示),蜡烛的火焰熄灭了.请解释其原因.
用粗铜丝绕成一个内径比蜡烛直径稍小一点的线圈,圈与圈之间有一定的空隙.点燃蜡烛,把铜丝制成的线圈从火焰上面罩下去,正好把蜡烛的火焰罩在铜丝里面(如图所示),蜡烛的火焰熄灭了.请解释其原因. 商场出售的服装都挂有面料成分及洗涤说明的标签,如图为某服装的标签.请回答.
商场出售的服装都挂有面料成分及洗涤说明的标签,如图为某服装的标签.请回答.