题目内容
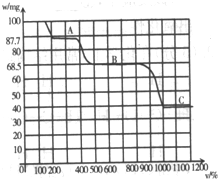 如图是100mgCaC2O4?H20受热时所得固体产物的质量随温度变化的曲线.试利用图中信息结合所学知识回答:
如图是100mgCaC2O4?H20受热时所得固体产物的质量随温度变化的曲线.试利用图中信息结合所学知识回答:
(1)推断CaC2O4?H20持续受热所得固体产物A、B、C的化学式;
(2)写出由A受热反应得到B的化学方程式.
解:根据题目要求可分3段讨论100mgCaC2O4?H20的受热分解.
??(1)t1时A点,100mgCaC2O4?H20的质量减少至87.7mg,从中分析CaC2O4?H20受热分解的产物,固体CaC2O4?H20的摩尔质量为146g/mol,设分解后产物的摩尔质量为M1.
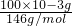 =
=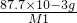 ?M1=128.04g/mol
?M1=128.04g/mol
??由于CaC2O4的摩尔质量为128g/mol,从而判断出CaC2O4?H20的分解反应方程式为:CaC2O4?H20 CaC2O4+H2O↑???A的化学式是CaC2O4.
CaC2O4+H2O↑???A的化学式是CaC2O4.
??再讨论t2时B点,87.7mg的CaC2O4受热分解,设分解产物的摩尔质量为M2.
?? =
=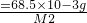 ,M2=99.98g/mol
,M2=99.98g/mol
从M2的实验值可推断出产物B应为CaCO3,分解方程式为CaC2O4 CaCO3+CO↑????
CaCO3+CO↑????
当加热至1100℃~1200℃时,由图读得分解产物C的质量约为38mg,设C点化合物摩尔质量为M3.
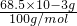 =
=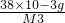 ?M3=55.47g/mol
?M3=55.47g/mol
??M3的实验值与CaO的摩尔质量(56g/mol)接近,分解方程式应为?CaCO3 CaO+CO2↑由此得出C的化学式为CaO,
CaO+CO2↑由此得出C的化学式为CaO,
综上分析,由A受热反应得到B的化学方程式为?CaC2O4 CaCO3+CO↑?
CaCO3+CO↑?
故答案为:
(1)A是CaC2O4,B是CaCO3,C是CaO
(2)CaC2O4 CaCO3+CO2↑
CaCO3+CO2↑
分析:对图象进行分析,从图中曲线变化分析推出不同温度下发生的化学反应,根据题目要求可分3段讨论100mgCaC2O4?H20的受热分解.
点评:本题通过固体受热分解曲线的图象告诉我们做化学题时一定要重视化学过程,从而培养化学意识,提高化学素质.
??(1)t1时A点,100mgCaC2O4?H20的质量减少至87.7mg,从中分析CaC2O4?H20受热分解的产物,固体CaC2O4?H20的摩尔质量为146g/mol,设分解后产物的摩尔质量为M1.
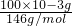 =
=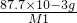 ?M1=128.04g/mol
?M1=128.04g/mol??由于CaC2O4的摩尔质量为128g/mol,从而判断出CaC2O4?H20的分解反应方程式为:CaC2O4?H20
 CaC2O4+H2O↑???A的化学式是CaC2O4.
CaC2O4+H2O↑???A的化学式是CaC2O4.??再讨论t2时B点,87.7mg的CaC2O4受热分解,设分解产物的摩尔质量为M2.
??
 =
=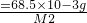 ,M2=99.98g/mol
,M2=99.98g/mol从M2的实验值可推断出产物B应为CaCO3,分解方程式为CaC2O4
 CaCO3+CO↑????
CaCO3+CO↑????当加热至1100℃~1200℃时,由图读得分解产物C的质量约为38mg,设C点化合物摩尔质量为M3.
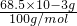 =
=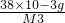 ?M3=55.47g/mol
?M3=55.47g/mol??M3的实验值与CaO的摩尔质量(56g/mol)接近,分解方程式应为?CaCO3
 CaO+CO2↑由此得出C的化学式为CaO,
CaO+CO2↑由此得出C的化学式为CaO,综上分析,由A受热反应得到B的化学方程式为?CaC2O4
 CaCO3+CO↑?
CaCO3+CO↑?故答案为:
(1)A是CaC2O4,B是CaCO3,C是CaO
(2)CaC2O4
 CaCO3+CO2↑
CaCO3+CO2↑分析:对图象进行分析,从图中曲线变化分析推出不同温度下发生的化学反应,根据题目要求可分3段讨论100mgCaC2O4?H20的受热分解.
点评:本题通过固体受热分解曲线的图象告诉我们做化学题时一定要重视化学过程,从而培养化学意识,提高化学素质.

练习册系列答案
相关题目
某化工厂用石灰石(杂质不溶于水,也不参加反应)、纯碱和水等原料来制烧碱溶液,再经过滤、蒸发等步骤制取固体烧碱.某化学兴趣小组要分析该化工厂仓库中放置一段时间后的固体烧碱样品成分,他们对烧碱样品的成分进行了如下猜测:
猜想:猜想一:该样品的成分可能只有氢氧化钠;
(1)猜想二:该样品中除了氢氧化钠外,还可能含有碳酸钠.支持这种猜测的依据是(用化学方程式表示)
①________②________.
猜想三:该样品中除了氢氧化钠外,还可能有氢氧化钙和碳酸钙.
猜想四:该样品中除了氢氧化钠外,还可能有氢氧化钙和碳酸钠
(2)实验与验证:他们设计实验进行探究,首先验证猜想一.进行的实验是:取少量固体样品配制成溶液,将少量溶液加入试管中,滴入酚酞,观察到试液变红.由此得出的结论是该样品只有氢氧化钠.他们又反思实验过程,觉得结论不正确,理由是________.
(3)他们验证猜想二,请你帮助完成实验表格.
| 实验步骤 | 现象 | 结论 |
| 取少量固体样品溶于水中,溶液澄清 | ----------------------------------- | --------------------------------------- |
| ①_______________ ②_______________ | ①_______________ ②_______________ | ①溶液中有碳酸钠 ②溶液中有氢氧化钠 |
________.