题目内容
3.(1)水是人类最宝贵的资源,可淡水资源短缺,所以雨水资源化是一种发展趋势.作为城市小主人的同学们请回答下列问题:①雨水在降落过程中常受到NO2、的污染形成酸雨,若要测定某雨水酸度,可使用pH试纸(或pH计).
②空气中的SO2主要来源于化石燃料的燃烧.
③收集的地面雨水常携带树叶、塑料袋等不溶杂物,处理雨水时应进行沉降和过滤.
④要使主要受SO2污染的酸雨可被回收利用,必须对其酸性进行中和,你认为较为经济有效的方法是加入适量的B固体.
A.NaCl B.Ca(OH)2 C.CaCl2 D.Na2CO3
(2)食品吸潮和吸氧后容易变质,为了延长食品保质期,通常在包装袋中加入1小包干燥剂.某化学兴趣小组经过查阅资料,发现某食品干燥剂的主要成分是生石灰.请回答下列问题:
①将装有干燥剂的小纸袋打开露置于潮湿的空气中,发现纸带发热,该反应的化学方程式为CaO+H2O═Ca(OH)2.该现象说明化学反应除了生成新物质外,还伴随着热量变化.
②小组在查阅资料中,还发现了一种新型的食品干燥剂:泡沫铁粉(铁粉包裹在泡沫塑料中).当它露置于潮湿的空气中,很快变成铁锈(主要成分为Fe2O3•nH2O). 与生石灰做干燥剂比较,泡沫铁粉除了能吸收水份做干燥剂外,还可做除氧剂.
分析 (1)测定溶液的酸碱度,可以使用PH试纸或PH计,二氧化硫能与水反应生成亚硫酸,要分离不溶性固体与液体,可以使用过滤的方法,酸雨能与碱性物质反应.
(2)①一种是以生石灰为主要成份的干燥剂,简称A类,结合生石灰与水反应生成氢氧化钙,进行分析解答.
②根据题意,泡沫铁粉(铁粉包裹在泡沫塑料中).当它露置于潮湿的空气中,很快变成铁锈(主要成分为Fe2O3•nH2O),并有发热现象,进行分析解答.
解答 解:(1)①要测定某雨水酸度,可使用PH试纸或PH计,所以本题答案为:pH试纸(或pH计);
②化石燃料中含有的硫燃烧能生成二氧化硫,二氧化硫与水反应生成亚硫酸,所以本题答案为:化石燃料的燃烧;
③要分离不溶性固体与液体,可以使用过滤的方法,所以本题答案为:过滤;
④酸雨能与碱性物质反应,A不与酸反应,C不与酸反应,D的价格高,故选B.
(2)①一种是以生石灰为主要成份的干燥剂,简称A类,生石灰与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2.并有发热现象,说明化学反应除了生成新物质外,还伴随着热量的变化.
②铁与氧气和水反应能生成铁锈,同时放出热量.泡沫铁粉除了能吸收水份做干燥剂外,还可做除氧剂.
答案:
(1)①pH试纸(或pH计);
②化石燃料的燃烧;
③过滤;
④B;
(2)①CaO+H2O═Ca(OH)2.热量;
②除氧.
点评 本题考查了酸雨的形成以及处理方法,完成此题,可以依据已有的知识进行.掌握生石灰的化学性质、化学变化中的能量变化等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.植被丰富的公园中有丰富的负氧离子,空气中氧分子得到电子就能形成负氧离子(O22-).下列关于O22-与O2的说法,错误的是( )
| A. | O22-与O2的化学性质不同 | B. | O22-与O2的电子总数不同 | ||
| C. | O22-与O2的质子数不同 | D. | O22-与O2的相对原子质量之和相同 |
11.实验室用高锰酸钾制氧气时,有如下操作步骤:①加热;②检查装置气密性;③装药品;④把试管固定在铁架台上;⑤把盛水的集气瓶倒立在水槽内;⑥熄灭酒精灯;⑦从水槽中取出导气管;⑧用排水法收集气体.则正确的操作顺序是( )
| A. | ③②④①⑧⑤⑥⑦ | B. | ②③④⑤①⑧⑦⑥ | C. | ②④③①⑤⑧⑦⑥ | D. | ②③④⑤①⑧⑥⑦ |
15.下列对如图所示各实验的分析不正确的是( )
| A. | 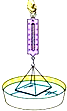 甲稍稍用力拉水平接触水面的玻璃板,测力计示数变大,说明分子间存在引力 | |
| B. | 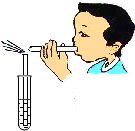 乙实验说明流体中流速越大的位置压强越小 | |
| C. | 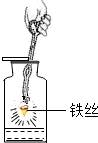 丙实验说明铁丝在氧气中燃烧生成氧化铁 | |
| D. | 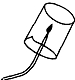 某气体燃烧,烧杯内壁出现水雾,说明该气体中含有氢元素 |
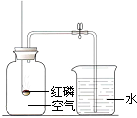 某同学用如图所示装置来测定空气中氧气的体积分数,请填写下列空白.
某同学用如图所示装置来测定空气中氧气的体积分数,请填写下列空白.


 已知:A、B、C、D、E、F六种物质是初中化学常见的物质.A、B是单质,C、D、E都是氧化物.A、B、C转化为F的过程较为复杂,F的成份也较复杂.其主要成分是一种红色的固体.试根据各物质间的转化关系完成下列各题.(题中除反应条件未给出外,反应物和产物均已给出.)
已知:A、B、C、D、E、F六种物质是初中化学常见的物质.A、B是单质,C、D、E都是氧化物.A、B、C转化为F的过程较为复杂,F的成份也较复杂.其主要成分是一种红色的固体.试根据各物质间的转化关系完成下列各题.(题中除反应条件未给出外,反应物和产物均已给出.)