题目内容
10. 硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:
硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:①t1℃时,两物质中溶解度较大的是氯化钾.
②t2℃时,两物质的等质量饱和溶液降温至t1℃,析出固体质量较大的是硝酸钾的溶液.
③t2℃时,将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的饱和(填“饱和”或“不饱和”)溶液.保持温度不变,往该烧杯中再加入10g水,充分搅拌后,氯化钾溶液的溶质的质量分数不变(填“变大”、“不变”或“变小”).
④欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是t≥t1.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:①通过分析溶解度曲线可知,t1℃时,两物质中溶解度较大的是氯化钾;
②硝酸钾的溶解度受温度变化影响较大,所以t2℃时,两物质的等质量饱和溶液降温至t1℃,析出固体质量较大的是硝酸钾的溶液;
③t2℃时,氯化钾的溶解度是40g,所以将100g水加入盛有50g氯化钾的烧杯中,充分溶解后,得到氯化钾的饱和溶液,保持温度不变,往该烧杯中再加入10g水,充分搅拌后,溶液仍然是饱和溶液,所以氯化钾溶液的溶质的质量分数不变;
④t1℃时,硝酸钾的溶解度是25g,饱和溶液的质量分数为$\frac{25g}{100g+25g}$×100%=20%,欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是t≥t1.
故答案为:①氯化钾;
②硝酸钾;
③饱和,不变;
④t≥t1.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
20.某化合物R与氧气放于密闭的容器中引燃,充分反应后,生成二氧化碳和水.实验测得的反应前后物质质量如表所示.
下列说法不正确的是( )
| 物质 | R | 氧气 | 二氧化碳 | 水 |
| 反应前质量/g | 51 | 96 | 0 | 0 |
| 反应后质量/g | x | 0 | 88 | 54 |
| A. | R中只含有碳氢元素 | |
| B. | x的值为5 | |
| C. | 该反应属于氧化反应 | |
| D. | 生成的二氧化碳和水分子个数比为2:3 |
1.氧气和二氧化碳在性质上的相似点是( )
①通常状况下都是气体②都能与碳反应③都可用于灭火④都是氧化物⑤都具有还原性⑥都易溶于水⑦标准状况下密度都比空气大.
①通常状况下都是气体②都能与碳反应③都可用于灭火④都是氧化物⑤都具有还原性⑥都易溶于水⑦标准状况下密度都比空气大.
| A. | ①②③④⑤⑥⑦ | B. | ①②④⑦ | C. | ①②⑥⑦ | D. | ①②⑦ |
18.将A,B两种物质各20g混合加热,B完全反应,生成16gC和8gD.则参加反应的A和B的质量比为( )
| A. | l:l | B. | 1:2 | C. | 1:5 | D. | 1:4 |
15.化学反应前后可能发生变化的是( )
| A. | 分子数目 | B. | 元素种类 | C. | 原子数目 | D. | 物质的总质量 |
19.下列有关氧气的叙述正确的是( )
| A. | 测定空气中氧气含量的实验中,可以将铜丝换成木炭 | |
| B. | 氧气的化学性质比较活泼,是可燃物 | |
| C. | 铁丝在氧气中剧烈燃烧,发出耀眼的白光,生成黑色固体 | |
| D. | 从空气中分离出的氮气可用于食品防腐 |
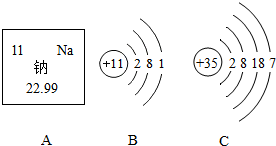 如图A是钠元素在周期表中的相关信息,B是钠元素原子结构示意图,C是溴元素(Br)原子结构示意图,回答问题.
如图A是钠元素在周期表中的相关信息,B是钠元素原子结构示意图,C是溴元素(Br)原子结构示意图,回答问题.