题目内容
5.将一定质量的铝放在氧气中燃烧后,称得剩余固体的质量比铝的质量增重了0.96克,求参加反应的铝的质量?(Al-27,O-16)分析 铝放在氧气中燃烧生成了氧化铝后,称得剩余固体的质量比铝的质量增重了0.96克,由质量守恒定律可知参加反应的氧气的质量为0.96g,据此可计算出参加反应铝的质量.
解答 解:由质量守恒定律可知,参加反应的氧气的质量为0.96g,
设参加反应的铝的质量为x
4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3
108 96
x 0.96g
$\frac{108}{96}=\frac{x}{0.96g}$ 解得x=1.08g.
答:参加反应的铝的质量是1.08g.
点评 本题属于根据化学方程式的简单计算,根据质量守恒定律判断出参加反应氧气的质量是解答本题的关键.

练习册系列答案
相关题目
13.现有两瓶无色溶液,一瓶是氢氧化钠溶液,另一瓶是石灰水,要鉴别出来,选用的试剂是( )
| A. | 酚酞溶液 | B. | 稀盐酸 | C. | 碳酸钠溶液 | D. | 氯化钙溶液 |
13.如图是物质E和G发生化学反应生成另外两种物质L和M的微观示意图,则下列有关说法错误的是( )
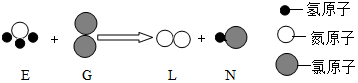

| A. | 一个E分子由4个原子构成 | B. | G物质和M物质都是单质 | ||
| C. | L、M分子是不断运动着的 | D. | M物质是由HCl分子构成的 |
20.下列说法能用质量守恒定律解释的是( )
| A. | mg水受热形成mg水蒸气 | |
| B. | 煤燃烧后留下的煤灰比原煤的质量少 | |
| C. | 10g食盐溶于70g水中得到80g食盐水 | |
| D. | 湿衣服凉干后,质量变小 |
10.下列物质间的转化不能一步完成的是( )
| A. | BaCl2→Ba SO4 | B. | CuO→Cu(OH)2 | C. | NaOH→Na2CO3 | D. | MgSO4→Mg(OH)2 |
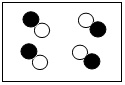
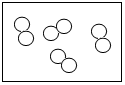

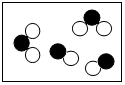


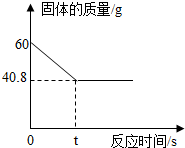 某学习小组在实验室中用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应过程中固体质量变化如图所示,请计算.
某学习小组在实验室中用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应过程中固体质量变化如图所示,请计算.