题目内容
(7分)氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程:
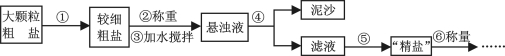
(1)操作①中必须用到的一种仪器是 (填序号)。
A.研钵 B.量筒 C.烧杯 D.试管
(2)完成该实验部分操作过程如图所示,其有明显错误 (填字母序号)。

(3)操作⑤中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取 等措施。
(4)用提纯得到的“精盐”配制了50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能
有 (填序号).
①氯化钠固体仍然不纯
②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
(5)查阅相关资料得知:粗盐中除含泥沙等不溶性杂质外,还含有少量的MgCl2、CaCl2等可溶性杂质;为了得到较纯净的氯化钠,除去泥沙的“精盐”又作了如下处理(假定杂质只有MgCl2、CaCl2两种)注:反应中所加试剂均过量
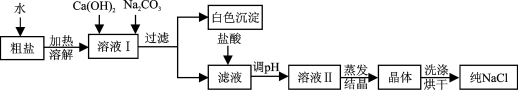
①白色沉淀含有物质的化学式为 ;
②在得到的滤液中加入过量盐酸的目的是 ;
③选用蒸发结晶法而不用降温结晶法的理由是 。
(1)A (2)AC (3)间歇加热(4)①②④
(5)①Mg(OH)2 CaCO3 ②除尽NaOH溶液、Na2CO3溶液 ③氯化钠的溶解度受温度的影响很小
【解析】
试题分析:大颗粒的固体变为小颗粒状的说明经过研磨,所以操作①中必须用到的一种仪器是研钵,取用固体是瓶盖要倒扣在桌面,防止污染药品,过滤要用玻璃棒引流,不能直接倒入漏斗内,操作⑤中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取间歇加热等方法,配制的质量分数偏小可能是因为氯化钠固体仍然不纯;称量时砝码端忘垫质量相同的纸片;装瓶时,有少量溶液洒出;量取水时,俯视读数等。白色沉淀含有物质的化学式根据提供的物质看应该是Mg(OH)2 CaCO3,在得到的滤液中加入过量盐酸的目的是除尽NaOH溶液、Na2CO3溶液,蒸发结晶法而不用降温结晶法的理由是氯化钠的溶解度受温度的影响很小
考点:溶液的配制 酸碱盐的性质和变化 粗盐的提纯 物质的溶解度


