题目内容
下表列出了20℃时KNO3溶解实验一组数据:
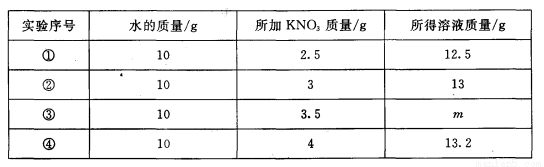
下列叙述中错误的是
A.①②所得溶液是不饱和溶液
B.③中m=13.2
C.④所得溶液的质量分数为32%
D.20℃时KNO3的溶解度为32g
C
【解析】
试题分析:根据表中数据可看出,当加入KNO3的质量4g时,所得溶液质量为13.2g,说明10g水最多只能溶解3.2g KNO3,A、①②所得溶液是不饱和溶液,正确,B、③中m=13.2,正确,C、④所得溶液的质量分数=32g/132g×100%=24.2%,错误,D、由于10g水最多只能溶解3.2g KNO3,故20℃时KNO3的溶解度为32g,正确,故选C
考点:溶解度的计算,饱和溶液、不饱和溶液的判断,溶质质量分数的计算

练习册系列答案
相关题目