题目内容
11.不停地加热一杯不饱和硝酸钾溶液,蒸发溶剂,以下关于溶液发生的变化正确的是( )| A. | 整个过程中,硝酸钾溶液的质量分数不断增大 | |
| B. | 整个过程中,硝酸钾的溶解度不断增大 | |
| C. | 整个过程中,始终不断有硝酸钾晶体析出 | |
| D. | 析出晶体后,温度不变,加热相同时间析出的晶体质量相同 |
分析 A.根据某温度下的饱和溶液中溶质的质量分数是固定值来分析;
B.根据硝酸钾的溶解度与温度的关系来分析;
C.根据不饱和溶液向饱和溶液的转化过程来分析;
D.根据饱和溶液蒸发相同质量的水时析出晶体质量相同来分析.
解答 解:A.当硝酸钾溶液达到饱和状态后,当恒温蒸发溶剂时,溶质的质量分数不变,错误;
B.加热时温度升高,当恒温时硝酸钾的溶解度不变,错误;
C.开始是不饱和溶液,加热不会有晶体析出,错误;
D.析出晶体后,温度不变,加热相同时间蒸发的水的质量相等,故析出的晶体质量相同,正确;
故选D.
点评 本题考查的是溶液的知识,完成此题,可以依据饱和溶液和不饱和溶液的转化以及溶解度的变化进行.

练习册系列答案
相关题目
5. 甲、乙、丙三种物质的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去).下列选项不能实现图示转化的是( )
甲、乙、丙三种物质的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去).下列选项不能实现图示转化的是( )
 甲、乙、丙三种物质的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去).下列选项不能实现图示转化的是( )
甲、乙、丙三种物质的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去).下列选项不能实现图示转化的是( )| 选项 | 甲 | 乙 | 丙 |
| A | H2SO4 | H2 | H2O |
| B | C | CO | CO2 |
| C | Ca(OH)2 | CaCl2 | CaCO3 |
| D | NaOH | NaCl | NaNO3 |
| A. | A | B. | B | C. | C | D. | D |
6.过氧化钠常用作呼吸面具里的供养剂.兴趣小组取适量过氧化钠粉末,加入到一定量水中,充分反应后,滴入几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,小组同学对此现象产生好奇.
【提出问题】什么原因导致溶液先变红再褪色
【查阅资料】过氧化钠(Na2O2)是一种浅黄白色颗粒粉末,在空气中吸收水分和二氧化碳,易溶于水,能与水发生反应生成氢氧化钠和过氧化氢.
【猜想与假设】猜想1:甲同学:“可能是无色酚酞溶液变质导致溶液褪色;”
猜想2:乙同学:“可能是生成的过氧化氢使溶液褪色.”
【实验与结论】(1)猜想1,其他同学一致认为不合理,理由是如果是无色酚酞溶液变质,刚开始就不会先变成红色了;
(2)乙同学设计了以下方案进行实验,证明自己的猜想:
【拓展】有同学从资料上得知氢氧化钠溶液浓度过大能导致溶液颜色褪去,他们又进行了以下的实验探究.
【提出问题】什么原因导致溶液先变红再褪色
【查阅资料】过氧化钠(Na2O2)是一种浅黄白色颗粒粉末,在空气中吸收水分和二氧化碳,易溶于水,能与水发生反应生成氢氧化钠和过氧化氢.
【猜想与假设】猜想1:甲同学:“可能是无色酚酞溶液变质导致溶液褪色;”
猜想2:乙同学:“可能是生成的过氧化氢使溶液褪色.”
【实验与结论】(1)猜想1,其他同学一致认为不合理,理由是如果是无色酚酞溶液变质,刚开始就不会先变成红色了;
(2)乙同学设计了以下方案进行实验,证明自己的猜想:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量稀氢氧化钠溶液于试管中,滴加1-2滴酚酞试液,变红后,往试管中滴加过氧化氢溶液,观察现象. | 溶液仍然为红色 | 不是过氧化氢使溶液褪色 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量原溶液于试管中,加入适量的水. | 溶液变成红色 | 氢氧化钠溶液浓度过大,导致溶液颜色褪去 |
1.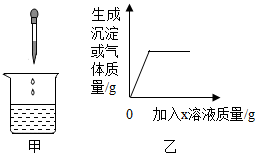 向烧杯中逐渐加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
向烧杯中逐渐加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
 向烧杯中逐渐加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
向烧杯中逐渐加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )| 烧杯中的物质 | X溶液 | |
| A | 稀硫酸 | 氯化钡溶液 |
| B | 氯化钠溶液 | 硝酸银溶液 |
| C | 硫酸和硫酸铜混合溶液 | 氢氧化钠溶液 |
| D | 碳酸氢钠溶液 | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |