题目内容
4.某钢样品的含碳量为0.24%(其他杂质元素不考虑),若碳元素主要以Fe2C和Fe3C的形式存在,则该钢样品中Fe2C和Fe3C的质量分数(w)范围是D(相对分子质量:Fe2C:124;Fe3C:180)A.0.03%<w<2% B.0.48%<w<0.72% C.2.24%<w<3.36% D.2.48%<w<3.6%
分析 这道题使用极限法即可正确解答.因为碳元素主要以Fe2C形式存在时质量最大,碳元素主要以Fe3C形式存在时质量最小.故用假设法分别求出碳元素主要以Fe2C形式存在时该钢样品中Fe2C和Fe3C的质量分数和碳元素主要以Fe3C形式存在时该钢样品中Fe2C和Fe3C的质量分数,就可得出取值范围.
解答 解:假设0.24%全部是Fe2C,则该钢样品中Fe2C和Fe3C的质量分数为0.24%÷$\frac{12}{124}$×100%=2.48%;
假设0.24%全部是Fe3C,则该钢样品中Fe2C和Fe3C的质量分数为0.24%÷$\frac{12}{180}$×100%=3.6%;
所以2.48%<ω<3.6%.
故选D.
点评 本题主要考查学生运用极限法和假设法和元素的质量分数公式解答问题的能力.一般要求取值范围的题,都可用极限法解答.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
16. 如图有一空心铜球悬浮在硫酸铜溶液中,且铜球不与烧杯内壁和底部接触,现向硫酸铜溶液中投入一小块铁,待铁块充分反应后(忽略溶液体积的变化),下列对铜球静止后的有关判断正确的是( )
如图有一空心铜球悬浮在硫酸铜溶液中,且铜球不与烧杯内壁和底部接触,现向硫酸铜溶液中投入一小块铁,待铁块充分反应后(忽略溶液体积的变化),下列对铜球静止后的有关判断正确的是( )
 如图有一空心铜球悬浮在硫酸铜溶液中,且铜球不与烧杯内壁和底部接触,现向硫酸铜溶液中投入一小块铁,待铁块充分反应后(忽略溶液体积的变化),下列对铜球静止后的有关判断正确的是( )
如图有一空心铜球悬浮在硫酸铜溶液中,且铜球不与烧杯内壁和底部接触,现向硫酸铜溶液中投入一小块铁,待铁块充分反应后(忽略溶液体积的变化),下列对铜球静止后的有关判断正确的是( )| A. | 漂浮 | B. | 浮力不变 | C. | 浮力变大 | D. | 沉到底部 |
13.硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,充分反应后有少量金属析出,过滤后往滤液中滴加盐酸,有白色沉淀生成.则析出的少量金属是( )
| A. | Cu | B. | Ag | C. | Cu和Ag | D. | Fe和Cu |

 ”“
”“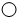 ”分别表示两种不同的原子,其中属于单质的是AB;属于化合物的是D;属于混合物的是C.
”分别表示两种不同的原子,其中属于单质的是AB;属于化合物的是D;属于混合物的是C.