题目内容
下列判断错误的是
- A.分子间的间隙:水蒸气>冰
- B.pH:碳酸钠溶液>氯化钠溶液
- C.碳元素的质量分数:C2H4<C3H6
- D.一个分子中原子总数:H2O2=NH3
C
分析:A、(一般的)分子间的间隙:气体>液体>固体;
B、碳酸钠溶液呈碱性,PH>7,氯化钠溶液溶液呈中性,PH=7;
C、分别求出两物质中的碳元素的质量分数,进行比较;
D、根据化学式H2O2,NH3;可以查出一个分子中原子总数.
解答:A、分子间的间隙:水蒸气>冰,判断正确,故A正确;
B、PH:碳酸钠溶液>氯化钠溶液,判断正确,因为碳酸钠溶液呈碱性,pH>7,故B正确;
C、C2H4碳元素的质量分数为 ×100%=
×100%=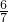 ×100%;C3H6碳元素的质量分数为
×100%;C3H6碳元素的质量分数为 ×100%=
×100%=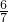 ×100%;所以碳元素的质量分数:H2O2=NH3,故C判断错误.
×100%;所以碳元素的质量分数:H2O2=NH3,故C判断错误.
D、一个分子中原子总数:H2O2=NH3,判断正确,故D正确.
故选C.
点评:了解利用原子和分子的性质分析和解决问题的方法;掌握溶液的酸碱盐与PH值的关系;掌握元素的质量分数的计算.
分析:A、(一般的)分子间的间隙:气体>液体>固体;
B、碳酸钠溶液呈碱性,PH>7,氯化钠溶液溶液呈中性,PH=7;
C、分别求出两物质中的碳元素的质量分数,进行比较;
D、根据化学式H2O2,NH3;可以查出一个分子中原子总数.
解答:A、分子间的间隙:水蒸气>冰,判断正确,故A正确;
B、PH:碳酸钠溶液>氯化钠溶液,判断正确,因为碳酸钠溶液呈碱性,pH>7,故B正确;
C、C2H4碳元素的质量分数为
 ×100%=
×100%=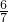 ×100%;C3H6碳元素的质量分数为
×100%;C3H6碳元素的质量分数为 ×100%=
×100%=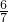 ×100%;所以碳元素的质量分数:H2O2=NH3,故C判断错误.
×100%;所以碳元素的质量分数:H2O2=NH3,故C判断错误.D、一个分子中原子总数:H2O2=NH3,判断正确,故D正确.
故选C.
点评:了解利用原子和分子的性质分析和解决问题的方法;掌握溶液的酸碱盐与PH值的关系;掌握元素的质量分数的计算.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一定条件下,在一个密闭容器中发生某反应,测得反应过程中物质的质量如下表所示:
|
物质 |
X |
Y |
Z |
Q |
|
第一次测得的质量/g |
68 |
16 |
4.4 |
3.6 |
|
第二次测得的质量/g |
4 |
未测 |
48.4 |
39.6 |
下列判断错误的是
A.第二次测定时Y已完全反应 B.若X为氧气,则Y发生氧化反应
C.该反应类型为化合反应 D.该反应中Z与Q质量变化之比为11:9


