题目内容
4.实验室现有质量分数为36.5%的浓盐酸,需要用它来配制质量分数为10%的稀盐酸73g,并用该稀盐酸来测定一包成分为Na2CO3和NaCl的白色固体中碳酸钠的质量分数.称取20g该白色固体放入烧杯中,加入上述稀盐酸,恰好完全反应.请回答下列问题:(1)配制质量分数为10%的稀盐酸73g所需上述浓盐酸的质量为20g.
(2)反应生成气体的质量为4.4g;
(3)求白色固体中碳酸钠的质量分数(写出计算过程).
分析 碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳;由参加反应的稀盐酸的质量、溶质的质量分数,由反应的化学方程式,列式计算出生成二氧化碳气体的质量、参加反应的碳酸钠的质量,据此进行分析解答.
解答 解:(1)设所需上述浓盐酸的质量为x,根据溶液稀释前后溶质的质量不变,
则73g×10%=x×36.5% x=20g.
(2)设生成二氧化碳气体的质量为x,参加反应的碳酸钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
y 73g×10% x
$\frac{73}{44}=\frac{73g×10%}{x}$ x=4.4g
(3)$\frac{106}{73}=\frac{y}{73g×10%}$ y=10.6g
白色固体中碳酸钠的质量分数为$\frac{10.6g}{20g}$×100%=53%.
答:(1)20;(2)4.4;(3)白色固体中碳酸钠的质量分数为53%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.欲除去下列物质中的少量杂质(括号内为杂质),所采取的方法正确的是( )
| 选项 | 物质 | 加入的试剂或操作 |
| A | NaCl 溶液(CaCl2) | 过量的碳酸钠溶液,过滤 |
| B | CaCO3(CaO) | 髙温煅烧 |
| C | Cu(NO3)2 溶液(AgN03) | 足量铜粉,过滤 |
| D | CO2(HC1) | 足量的氢氧化钠溶液,洗气 |
| A. | A | B. | B | C. | C | D. | D |
10.将3.52g CO2和SO2混合气体通入一定量的NaOH溶液中,气体全部与NaOH反应生成盐,将反应后的溶液减压低温蒸干后得到不含结晶水的固体,固体的质量可能为( )
| A. | 8.48 g | B. | 7.48 g | C. | 5.72 g | D. | 5.22g |
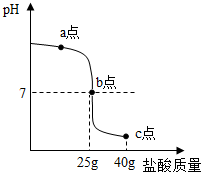 利用中和反应可以测定酸或碱溶液中溶质的质量分数.向20g溶质质量分数为4%的氢氧化钠溶液中不断滴加40g稀盐酸.
利用中和反应可以测定酸或碱溶液中溶质的质量分数.向20g溶质质量分数为4%的氢氧化钠溶液中不断滴加40g稀盐酸.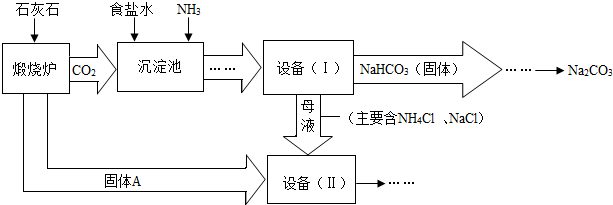
 某蔬菜基地如图所示,请回答:
某蔬菜基地如图所示,请回答: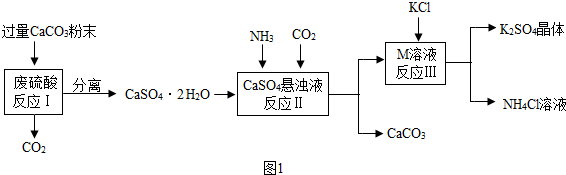
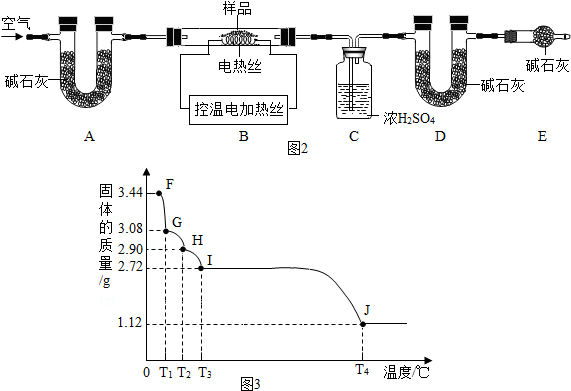
 A、B、C、D、E、F是初中化学常见的物质,A,B是含有相同元素的无色液体,D是最轻的气体,F是红色固体单质.根据如图的相互转化关系判断.
A、B、C、D、E、F是初中化学常见的物质,A,B是含有相同元素的无色液体,D是最轻的气体,F是红色固体单质.根据如图的相互转化关系判断.