题目内容
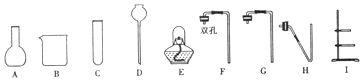
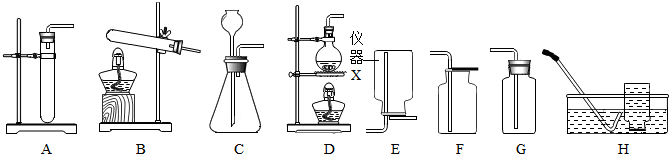
4.根据如图实验装置图进行气体制取和性质实验的探究: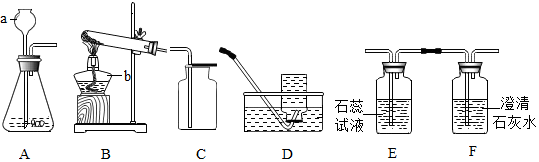
(1)写出仪器a的名称:长颈漏斗;
(2)实验室里不使用催化剂制取氧气时,可选用的发生装置是B(填字母代号,下同),发生反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;实验室收集CO2一般不选用D装置的原因是二氧化碳能溶于水,且与水反应.同学用图中A、E、F装置组合制备CO2气体并验证相关性质,则装置A应该先连接装置E(填E或F);E装置中发生反应的化学方程式为CO2+H2O=H2CO3;
(3)若装置A中的反应过于剧烈,从安全角度考虑,可以采取的措施有bd(填字母)
a、用容积较小的锥形瓶 b、将长颈漏斗换成针筒减慢液体的滴加速度
c、加热反应物 d、降低液体反应物的浓度
(4)盐酸中的溶质是氯化氢,实验室常用加热氯化钠固体与浓硫酸的混合物的方法来制取氯化氢气体.在实验室制取氯化氢气体时,不能(填“能”或“不能”)使用B装置作为气发生装置;发生反应的化学方程式为:2NaCl+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+2HCl↑.
分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.
解答 解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)如果用高锰酸钾制氧气就需要加热,也不需要催化剂,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;验室收集CO2一般不选用D装置的原因是:二氧化碳能溶于水,且与水反应;同学用图中A、E、F装置组合制备CO2气体并验证相关性质,则装置A应该先连接装置E;E中二氧化碳和水生成碳酸;故答案为:B;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;二氧化碳能溶于水,且与水反应;E;CO2+H2O=H2CO3;
(3)若装置A中的反应过于剧烈,从安全角度考虑,可以采取的措施有:将长颈漏斗换成针筒减慢液体的滴加速度;降低液体反应物的浓度;故答案为:bd;
(4)在实验室制取氯化氢气体时,不能使用B装置作为气发生装置,因为浓硫酸是液体;氯化钠固体与浓硫酸在加热的条件下生成硫酸钠和氯化氢气体,配平即可;故答案为:不能;2NaCl+浓H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+2HCl↑;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的检验和性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案(1)问题:通过有关实验证明生石灰能与水发生化学反应.
(2)资料收集:氧化钙能与水反应放出大量的热,氢氧化钙的水溶液能使酚酞试液变红
(3)提出猜测:氧化钙能与水反应生成氢氧化钙
(4)填写如表:
| 实验步骤 | 观察到的现象 | 分析和结论 |
| A. | ①⑤⑥ | B. | ③④⑥ | C. | ②③⑥ | D. | ①③④ |
①取5只250毫升集气瓶,向5只集气瓶中分别装入25毫升、50毫升、75毫升、100毫升、125毫升的水,并用毛玻璃片盖住,依次编号为1、2、3、4、5.
②用分解过氧化氢(H2O2)的方法制取氧气,通过排水法将上述1~5号瓶中的水排去.
③将带火星的木条依次插入1~5号瓶中,把观察到的现象和计算数据,填入下表.
| 集气瓶标号 | 1 | 2 | 3 | 4 | 5 |
| 集气瓶中氧气的体积分数 | 28.9% | 36.8% | 44.7% | 52.6% | 60.5% |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
(1)根据上述实验,下列说法中正确的是(B)
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条一定能复燃
C.只要有氧气存在就可使带火星的木条复燃
(2)上述实验表明:物质燃烧的剧烈程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈.请你再举一例,将实验内容和实验现象填写在下表中:
| 实验内容 | 实验现象 | 实验结论 |
| 分别取相同质量的硫粉,放在空气中和氧气中燃烧 | 硫在氧气中燃烧更剧烈 | 氧气浓度越大,燃烧越剧烈 |