题目内容
下表是NaCl、NH4Cl在不同温度时的溶解度.
①在80℃时NH4Cl的溶解度为 ,以上两种物质溶解度的变化受温度影响较小的是 .
②20℃时,将40gNaCl加入到100g水中充分搅拌后,所得溶液的质量为 g.
(2)如图是熟石灰的溶解度曲线图,请依据图示信息回答有关问题:
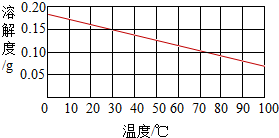
①熟石灰的溶解度随着温度升高而 (填“增大”或“降低”).
②在其他条件不变的情况下,若将20℃时熟石灰的饱和溶液升温至50℃,溶质的质量分数将 (填“变大”、“变小”或“不变”).
③可以使接近饱和的熟石灰溶液变成饱和溶液的方法是: (任写一种).
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
②20℃时,将40gNaCl加入到100g水中充分搅拌后,所得溶液的质量为
(2)如图是熟石灰的溶解度曲线图,请依据图示信息回答有关问题:

①熟石灰的溶解度随着温度升高而
②在其他条件不变的情况下,若将20℃时熟石灰的饱和溶液升温至50℃,溶质的质量分数将
③可以使接近饱和的熟石灰溶液变成饱和溶液的方法是:
考点:固体溶解度的影响因素,饱和溶液和不饱和溶液相互转变的方法,固体溶解度曲线及其作用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)
①根据观察图表可以看出:80℃时NH4Cl的溶解度;氯化钠的溶解度受温度影响较小解答;
②根据20℃时氯化钠的溶解度是36g分析解答;
(2)
①从图直接看出;
②根据熟石灰溶解度随温度的变化和质量分数公式分析;
③根据饱和溶液和不饱和溶液之间的转化方法分析.
①根据观察图表可以看出:80℃时NH4Cl的溶解度;氯化钠的溶解度受温度影响较小解答;
②根据20℃时氯化钠的溶解度是36g分析解答;
(2)
①从图直接看出;
②根据熟石灰溶解度随温度的变化和质量分数公式分析;
③根据饱和溶液和不饱和溶液之间的转化方法分析.
解答:解:
(1)
①观察图表可以看出:在80℃时NH4Cl的溶解度为65.6g;氯化钠的溶解度受温度影响较小;
②观察图表可以看出20℃时氯化钠的溶解度是36g,即20℃时100g水中最多溶解氯化钠36g;所以将40gNaCl加入到100g水中充分搅拌后,所得溶液的质量为136g;
(2)
①从图直接看出,熟石灰的溶解度随着温度升高而降低.故答案为:降低
②从图直接看出,熟石灰的溶解度随着温度升高而降低.在其他条件不变的情况下,若将20℃时熟石灰的饱和溶液升温至50℃时,将有固体析出,因此溶质的质量分数变小.故答案为:变小
③从图直接看出,熟石灰的溶解度随着温度升高而降低,因此使接近饱和的熟石灰溶液变成饱和溶液的方法有:①加溶质熟石灰②恒温蒸发水③升温.故答案为:加溶质熟石灰
答案:
(1)①65.6g NaCl ②136
(2)①降低 ②变小 ③加溶质熟石灰
(1)
①观察图表可以看出:在80℃时NH4Cl的溶解度为65.6g;氯化钠的溶解度受温度影响较小;
②观察图表可以看出20℃时氯化钠的溶解度是36g,即20℃时100g水中最多溶解氯化钠36g;所以将40gNaCl加入到100g水中充分搅拌后,所得溶液的质量为136g;
(2)
①从图直接看出,熟石灰的溶解度随着温度升高而降低.故答案为:降低
②从图直接看出,熟石灰的溶解度随着温度升高而降低.在其他条件不变的情况下,若将20℃时熟石灰的饱和溶液升温至50℃时,将有固体析出,因此溶质的质量分数变小.故答案为:变小
③从图直接看出,熟石灰的溶解度随着温度升高而降低,因此使接近饱和的熟石灰溶液变成饱和溶液的方法有:①加溶质熟石灰②恒温蒸发水③升温.故答案为:加溶质熟石灰
答案:
(1)①65.6g NaCl ②136
(2)①降低 ②变小 ③加溶质熟石灰
点评:了解溶解度的含义、饱和溶液和不饱和溶液相互转化方法,以及观察图表信息、并能用来分析解题是解答此题的关键.

练习册系列答案
相关题目
如图所示的实验操作中正确的是( )
A、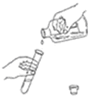 倾倒液体 |
B、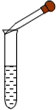 滴加液体 |
C、 加热液体 |
D、 读取液体体积 |
下列仪器不宜用来加热的是( )
| A、燃烧匙 | B、量筒 | C、烧杯 | D、试管 |