题目内容
8.NaCl、KNO3、Ca(OH)2三种物质的溶解度曲线如图一与图二所示.请回答:
(1)由图一可知,50℃时氯化钠的溶解度(填“>”或“<”)<硝酸钾的溶解度;
(2)欲对含有少量氯化钠的硝酸钾固体进行提纯,可以使用的提纯方法是降温结晶(或冷却热饱和溶液);
(3)20℃时,将20g氯化钠溶于50g水中,所得溶液的溶质质量分数为26.5%(保留一位小数);
(4)如图三所示,20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入氢氧化钠固体后,试管中出现的现象是石灰水变浑浊,结合图二分析其原因是氢氧化钠固体溶于水放热,而氢氧化钙的溶解度随温度升高而逐渐减小,所以有固体析出.
分析 (1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)据硝酸钾和氯化钠的溶解度受温度影响情况分析解答;
(3)据该温度下溶解度及溶质的质量分数解答;
(4)据氢氧化钠固体溶于水放热和氢氧化钙的溶解度随温度升高而减小分析解答.
解答 解:(1)由图一可知,50℃时氯化钠的溶解度小于硝酸钾的溶解度;
(2)硝酸钾的溶解度受温度影响较大,而氯化钠的溶解度受温度影响较小,所以欲对含有少量氯化钠的硝酸钾固体进行提纯,可以使用降温结晶或冷却热饱和溶液的提纯方法;
(3)20℃时氯化钠的溶解度是36g,即100g水中最多溶解36g的氯化钠,所以将20g氯化钠溶于50g水中,最,多溶解18g所得溶液的溶质质量分数为:$\frac{18g}{68g}$×100%≈26.5%;
(4)如图三所示,20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入氢氧化钠固体后,试管中石灰水会变浑浊;
结合图二分析其原因是:向水中加入氢氧化钠固体后,氢氧化钠溶于水放热,温度升高,氢氧化钙的溶解度随温度的升高而减少,因此石灰水变浑浊;
故答案为:(1)<;
(2)降温结晶(或冷却热饱和溶液);
(3)26.5%;
(4)石灰水变浑浊;氢氧化钠固体溶于水放热,而氢氧化钙的溶解度随温度升高而逐渐减小,所以有固体析出.
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,能较好考查学生分析、解决问题的能力.

练习册系列答案
相关题目
19.氯化钠是重要的盐.下列做法或说法中错误的是( )
| A. | 氯化钠的溶解度受温度变化的影响很小 | |
| B. | 在“一定溶质质量分数的氯化钠溶液的配制”的实验中,使用玻璃棒搅拌,加快氯化钠的溶解 | |
| C. | 氯化钠的水溶液能导电是因为氯化钠在水中会解离出能自由移动的Na+和Cl- | |
| D. | 在“粗盐中难溶性杂质的去除”的实验中,当蒸发皿中的滤液全部蒸干后才能停止加热 |
3.下列各种行为中,符合“绿色化学”理念的是( )
| A. | 提倡使用煤作燃料 | B. | 提倡使用甲醛溶液浸泡水产品 | ||
| C. | 提倡使用清洁能源 | D. | 提倡出行时多使用私家车 |
20.下列离子能在pH=2的水溶液中大量共存的是( )
| A. | Cl-、NO3-、K+、Na+ | B. | SO42-、NO3-、K+、OH- | ||
| C. | CO32-、SO42-、Mg2+ | D. | NH4+、Cl-、OH-、K+ |
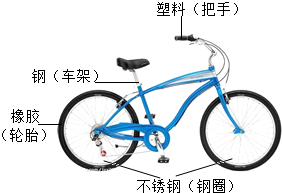 自行车作为常用的代步工具,既轻便灵活,又符合环保要求,有图是一款自行车的示意图.
自行车作为常用的代步工具,既轻便灵活,又符合环保要求,有图是一款自行车的示意图.  A、B、C、D是初中化学常见的物质,且为不同类别的化合物,A、B中都含有钙元素,它们之间的反应或转化关系如图所示(部分反应物、生成物及反应条件已略去)
A、B、C、D是初中化学常见的物质,且为不同类别的化合物,A、B中都含有钙元素,它们之间的反应或转化关系如图所示(部分反应物、生成物及反应条件已略去)