题目内容
4.化学改变世界的途径是使物质发生化学变化.下列变化属于化学变化的是( )| A. |  冰雪融化 | B. |  品红在水中扩散 | C. |  铁水铸成锅 | D. |  燃料的燃烧 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成.
解答 解:A、冰雪融化只是状态发生了变化,没有新物质生成,属于物理变化;
B、品红扩散的过程没有新物质生成,属于物理变化;
C、铁水铸成锅过程中没有新物质生成,属于物理变化;
D、燃料的燃烧过程中有二氧化碳等新物质生成,属于化学变化;
故选D.
点评 判断变化是否属于化学变化的唯一标准是:是否有新物质生成,如果有新物质生成,就是化学变化,如果没有新物质生成,就不是化学变化.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列各组物质能在水溶液中大量共存的是( )
| A. | HCl、NaOH、H2SO4 | B. | AgNO3、HNO3、BaCl2 | ||
| C. | Fe2(SO4)3、NaCl、KOH | D. | FeCl3、Na2SO4、KNO3 |
15.如图实验装置进行的相应实验,达不到实验目的是( )
| A. |  用如图所示装置除去CO2中含有的少量HCl气体 | |
| B. | 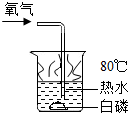 用如图所示的装置证明可燃物燃烧需要与氧气接触 | |
| C. | 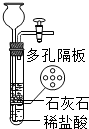 用如图所示装置制取少量CO2气体 | |
| D. |  在实验室中,用如图所示装置除去少量黄河水中的泥沙 |
12.元素周期表是学习和研究化学的重要工具.请下表(元素周期表的部分内容)回答有关问题:
(1)请从上表中查出关于硼元素的一条信息:硼的元素符号为B.
(2)第3周期(横行)中属于金属元素的是钠(填一种),其阳离子是Na+(填符号).
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(填“分子”或“原子”或“离子”).
(4)在元素周期中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是BD(填字母序号).
A.C和Ne B.Be和Mg C.Al和Si D.F和Cl
(5)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如AB(填字母序号).
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | 3Li 锂 6.941 | 4Be 铍 9.012 | 5B 硼 10.81 | 6C 碳 12.01 | 7N 氮 14.01 | 8O 氧 16.00 | 9F 氟 19.00 | 10Ne 氖 20.18 |
| 3 | 11Na 钠 22.99 | 12Mg 镁 24.31 | 13Al 铝 26.98 | 14Si 硅 28.09 | 15P 磷 30.97 | 16S 氯 32.06 | 17Cl 氯 35.45 | 18Ar 氩 39.95 |
(2)第3周期(横行)中属于金属元素的是钠(填一种),其阳离子是Na+(填符号).
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(填“分子”或“原子”或“离子”).
(4)在元素周期中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是BD(填字母序号).
A.C和Ne B.Be和Mg C.Al和Si D.F和Cl
(5)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如AB(填字母序号).
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同.
9.阿司匹林也叫乙酰水杨酸,是一种历史悠久的解热镇痛药.其化学式为C9H804,下列说法错误的是( )
| A. | 阿司匹林的一个分子由9个碳原子、8个氢原子和4个氧原子构成 | |
| B. | 阿司匹林由碳、氢、氧三种元素组成 | |
| C. | 阿司匹林中碳、氢、氧一种元素的质量比为27:2:16 | |
| D. | 阿司匹林的相对分子质量为180g |
13.亚硒酸钠(Na2SeO3)能消除加速人体衰老的活性氧,亚硒酸钠中硒元素(Se)的化合价为( )
| A. | -3 | B. | 0 | C. | +1 | D. | +4 |
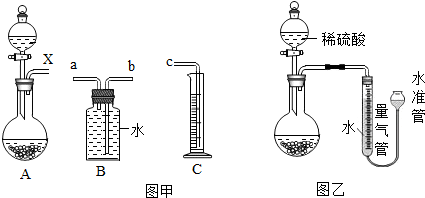
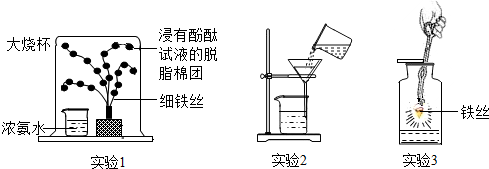
14.下面是某化学兴趣小组的同学对氢氧化钠部分性质的探究过程:
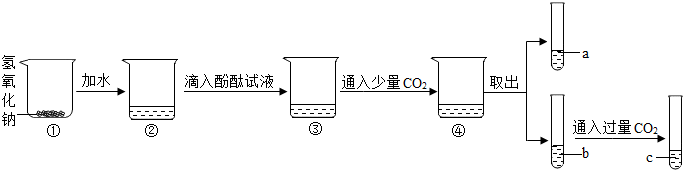
(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会放热(填“吸热”或“放热”),该溶液呈无色;③中的溶液显红色.
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈碱性(填“酸”或“碱”).
(3)c溶液和a溶液对比,c溶液颜色更浅.
【提出问题】为什么继续通入过量的二氧化碳气体溶液颜色会更浅?
【查阅资料】(1)Na2CO3+CO2+H2O═2NaHCO3 (2)Ca(NO3)2溶液与NaHCO3溶液不反应
【设计实验】
【实验结论】根据甲、乙两个实验得出的结论,写出甲实验中发生反应的化学方程式:NaHCO3+HCl=NaCl+H2O+CO2↑.
【实验反思】同种反应物在不同的条件下发生化学反应时,可能得到不同的产物.如:碳在氧气中燃烧可以生成二氧化碳或一氧化碳.

(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会放热(填“吸热”或“放热”),该溶液呈无色;③中的溶液显红色.
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈碱性(填“酸”或“碱”).
(3)c溶液和a溶液对比,c溶液颜色更浅.
【提出问题】为什么继续通入过量的二氧化碳气体溶液颜色会更浅?
【查阅资料】(1)Na2CO3+CO2+H2O═2NaHCO3 (2)Ca(NO3)2溶液与NaHCO3溶液不反应
【设计实验】
| 实验操作 | 实验现象 | 实验结论 | |
| 甲 | 取少量c溶液滴入稀盐酸 | 产生气泡 | 溶液中含较多的CO32-或HCO3- |
| 乙 | 另取少量c溶液滴入硝酸钙溶液 | 无明显现象 | 溶液中没有大量的碳酸根离子 |
【实验反思】同种反应物在不同的条件下发生化学反应时,可能得到不同的产物.如:碳在氧气中燃烧可以生成二氧化碳或一氧化碳.