题目内容
16.我国早在商朝就制造出青铜器,春秋时期开始炼铁,近几十年来铝业飞速发展.(1)青铜是铜和锡的合金,青铜属于金属材料.
(2)铁锅被广泛应用,主要是利用铁具有导热性.
(3)将Al和Fe的混合粉末加入到一定量的AgNO3溶液中,充分反应后,过滤,得到滤渣和浅绿色滤液,写出发生反应的化学方程式Al+3AgNO3=Al(NO3)3+3Ag、Fe+2AgNO3=Fe(NO3)2+2Ag(一个方程式两分),则滤渣中一定没有Al(填化学式),滤液中的溶质一定有Al(NO3)3、Fe(NO3)2(填化学式).
(4)生活中铁制品容易锈蚀,请说出自行车链条防锈常用的方法涂油.
分析 根据已有的金属的性质以及金属活动性顺序的意义进行分析解答,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此解答.
解答 解:(1)青铜属于合金,是金属材料,故填:金属;
(2)利用铁的导热性,可以用于铁锅,故填:导热;
(3)在金属活动性顺序中,Al>Fe>Ag,故铝和铁都能与硝酸银溶液反应,且铝先与硝酸银溶液反应,由于得到的是浅绿色滤液,故铁参与了反应,说明铝全部反应,铝与硝酸银反应生成的是硝酸铝和银,铁与硝酸银反应生成的是硝酸亚铁和银,说明滤渣中一定不含有铝,滤液中一定含有硝酸铝和硝酸亚铁,故填:Al+3AgNO3=Al(NO3)3+3Ag,Fe+2AgNO3=Fe(NO3)2+2Ag,Al,Al(NO3)3、Fe(NO3)2;
(4)自行车链条通常采用涂油的方法防锈,故填:涂油.
点评 本题考查的是金属的性质以及金属活动性顺序的应用,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
19.下列符号中,表示两个氢原子的是( )
| A. | H2 | B. | 2H2 | C. | 2H | D. | 2H+ |
20.“庄稼一枝花,全靠肥当家”.下列物质可作为氮肥的是( )
| A. | CaCl2 | B. | Ca(H2PO4)2 | C. | K2SO4 | D. | NH4HCO3 |
4.3月29日是本年度的“地球一小时”(Earth Hour)活动日,主题为“能见蔚蓝”,“能”意味着可再生能源能够带来改变,“蔚蓝”代表每个人对告别雾霾、寻回蓝天的期待,应对当前中国最紧迫.最受关注的环境议题--雾霾.作为一名中学生,下列做法不符合这一主题的是( )
| A. | 选择自行车和公交车作为出行工具 | |
| B. | 人走灯灭、节约用纸 | |
| C. | 将废纸、汽水瓶等收集起来,一次性焚烧 | |
| D. | 拒绝使用一次性木筷、用电子贺卡代替纸制贺卡 |
11.如表是日常生活中常用各种清洗剂.
(1)使用洗涤灵清洗餐具上的油污,这是因为它具有乳化功能.
(2)清除以下物质,可使用洁厕灵的是AC(填字母序号).
A.铁锈 B.油污 C.水垢 D.木炭还原氧化铜后,试管内壁残余的红色固体
(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2.若加入污渍爆炸盐以后,再加入洁厕灵,会造成去渍效果的降低,反应的化学方程式Na2CO3 +2HCl=2NaCl+H2O+CO2↑.
(4)将洁厕灵滴入炉具清洁剂中,如图甲所示.
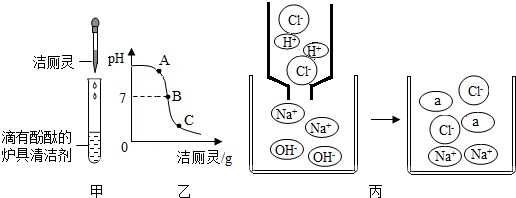
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外)NaCl、NaOH,此时溶液可用图乙中A(选填A、B、C)点处表示.
②若反应后溶液pH为7,图丙中a微粒的化学式为H2O.
③丙中反应没有明显现象,为证明反应发生,可加入的试剂有A.
A.无色酚酞溶液 B.硝酸钾溶液 C.硝酸银溶液 D.锌粒
(5)“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(-O-O-).据此推测,如表物质中,可用作杀菌消毒剂的是D(填序号).
| 名称 | 洗涤灵 | 洁厕灵 | 炉具清洁剂 | 活氧彩漂 | 污渍爆炸盐 |
| 产品样式 |  |  |  |  |  |
| 有效成分或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过氧化氢 | 过碳酸钠 |
(2)清除以下物质,可使用洁厕灵的是AC(填字母序号).
A.铁锈 B.油污 C.水垢 D.木炭还原氧化铜后,试管内壁残余的红色固体
(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2.若加入污渍爆炸盐以后,再加入洁厕灵,会造成去渍效果的降低,反应的化学方程式Na2CO3 +2HCl=2NaCl+H2O+CO2↑.
(4)将洁厕灵滴入炉具清洁剂中,如图甲所示.

①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外)NaCl、NaOH,此时溶液可用图乙中A(选填A、B、C)点处表示.
②若反应后溶液pH为7,图丙中a微粒的化学式为H2O.
③丙中反应没有明显现象,为证明反应发生,可加入的试剂有A.
A.无色酚酞溶液 B.硝酸钾溶液 C.硝酸银溶液 D.锌粒
(5)“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(-O-O-).据此推测,如表物质中,可用作杀菌消毒剂的是D(填序号).
| H-O-H | 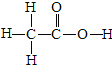 | O=C=O | 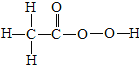 |
| A | B | C | D |
1.下列实验操作正确的是( )
| A. | 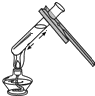 加热液体 | B. | 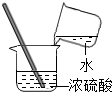 稀释浓硫酸 | C. |  检验气密性 | D. |  熄灭酒精灯 |
8.空气是人类宝贵的自然资源.下列有关空气的说法错误的是( )
| A. | 氧气可用作火箭发射的燃料 | |
| B. | 液氮可用作制冷剂 | |
| C. | 氦气可用来填充探空气球 | |
| D. | 二氧化碳是植物进行光合作用必需的物质 |
6.20℃时,将等质量不含结晶水的甲、乙固体分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3,下列说法错误的是( )
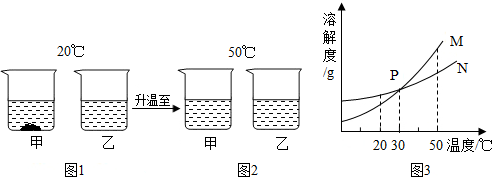

| A. | 图1中,乙一定是饱和溶液 | |
| B. | 图2中,两溶液中溶质的质量分数一定相等 | |
| C. | 图3中,M表示甲的溶解度曲线 | |
| D. | 图2中,两溶液降温至30℃一定都不会析出晶体 |
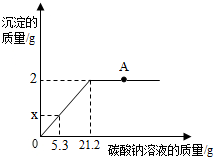 某盐场生产的食盐产品中含有氯化钙杂质,某化学兴趣小组为测定该食品产品中氯化钠的质量分数,进行了如下实验:取100g食盐样品完全溶解于水,逐渐加入碳酸钠溶液,反应关系如图所示:
某盐场生产的食盐产品中含有氯化钙杂质,某化学兴趣小组为测定该食品产品中氯化钠的质量分数,进行了如下实验:取100g食盐样品完全溶解于水,逐渐加入碳酸钠溶液,反应关系如图所示: