题目内容
14. 某补钙剂说明书的部分信息如图所示.小明对该补钙剂十分感兴趣,取10片钙片放入90g稀盐酸中,有效成分刚好完全反应(其他成分不与盐酸反应).剩余固体和液体总质量为97.8g.请完成下列问题:
某补钙剂说明书的部分信息如图所示.小明对该补钙剂十分感兴趣,取10片钙片放入90g稀盐酸中,有效成分刚好完全反应(其他成分不与盐酸反应).剩余固体和液体总质量为97.8g.请完成下列问题:(1)反应生成了二氧化碳气体2.2g;
(2)10片钙片中CaCO3的质量是多少克?(写出计算过程)
分析 根据题干提供的信息结合标签进行分析,混合物减少的质量就是生成的二氧化碳的质量,根据二氧化碳的质量结合反应的化学方程式就可以求出碳酸钙的质量,据此解答.
解答 解:(1)混合物减少的质量就是生成的二氧化碳的质量,所以生成的二氧化碳的质量是10g+90g-97.8g=2.2g;
(2)设钙片中CaCO3的质量是x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
$\frac{100}{x}=\frac{44}{2.2g}$
x=5g
故答案为:
(1)2.2;
(2)10片钙片中CaCO3的质量是5g.
点评 本题考查了根据化学方程式的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
9.物质的用途和性质密切相关.下列用途主要是利用其化学性质的是( )
| A. |  活性炭用于防毒面具 | B. |  金刚石作装饰品 | ||
| C. |  石墨制铅笔 | D. |  二氧化碳灭火 |
3.地壳中含量最多的元素和地壳中含量最多的金属元素及空气中含量最多的元素形成的化合物的化学式是( )
| A. | Al2O3 | B. | Na2SiO3 | C. | Al(NO3)3 | D. | Fe(NO3)3 |
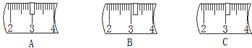
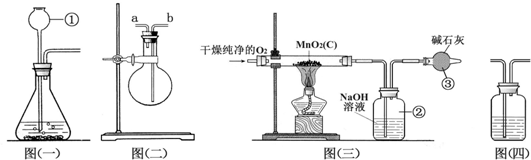
 某化学兴趣小组的同学对教材中“测定空气里氧气含量”的实验进行了大胆的改进,设计了如图所示的实验装置,请你积极参与,并回答下列问题:
某化学兴趣小组的同学对教材中“测定空气里氧气含量”的实验进行了大胆的改进,设计了如图所示的实验装置,请你积极参与,并回答下列问题: