题目内容
某同学为了验证质量守恒定律,将镁条在空气中点燃,结果发现燃烧后生成物的质量比原来镁条的质量增大,由此得出这个化学反应不遵守质量守恒定律的结论.你认为这个结论正确吗?为什么?
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据镁条在空气中燃烧的化学方程式进行分析.根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.
解答:解:
不正确;因为镁条在空气中燃烧,就是与空气中的氧气发生反应生成氧化镁的过程,则化学方程式为:2Mg+O2
2MgO.根据质量守恒定律,生成物的质量=镁条的质量+参与反应的氧气质量,所以生成物的质量比原来镁条的质量增加了.
故答案为:不正确,因为参加反应的镁和氧气的质量总和等于反应后生成的氧化镁质量,因此这个化学反应遵守质量守恒定律.
不正确;因为镁条在空气中燃烧,就是与空气中的氧气发生反应生成氧化镁的过程,则化学方程式为:2Mg+O2
| ||
故答案为:不正确,因为参加反应的镁和氧气的质量总和等于反应后生成的氧化镁质量,因此这个化学反应遵守质量守恒定律.
点评:本题主要考查学生运用质量守恒定律解答问题的能力,关键是强调物质的质量总和.

练习册系列答案
相关题目
下列四种溶液敞口放置在空气中,质量因发生化学变化而减小的是( )
| A、NaOH溶液 |
| B、Ca(OH)2溶液 |
| C、浓盐酸 |
| D、浓硫酸 |
水是生命之源,以下生活中的“水”能看成纯净物的是( )
| A、矿泉水 | B、结冰的海水 |
| C、自来水 | D、结冰的蒸馏水 |
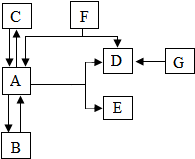 自然界中存在着氧循环、碳循环、水循环等.如图为水循环,其中A、B、C是水循环中水的三种自然状态,A为密度最大时的状态.D能支持燃烧并能与许多物质发生氧化反应.G是暗紫色固体,加热时生成D和另两种固体,其中一种固体可作F分解反应的催化剂.试回答下列问题:
自然界中存在着氧循环、碳循环、水循环等.如图为水循环,其中A、B、C是水循环中水的三种自然状态,A为密度最大时的状态.D能支持燃烧并能与许多物质发生氧化反应.G是暗紫色固体,加热时生成D和另两种固体,其中一种固体可作F分解反应的催化剂.试回答下列问题: