题目内容
某兴趣小组同学用65克锌与足量的稀硫酸反应制取氢气,请问产生氢气的质量为多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:锌和稀硫酸反应生成硫酸锌和氢气,根据锌的质量可以计算生成氢气的质量.
解答:解:设生成氢气的质量为x,
Zn+H2SO4═ZnSO4+H2↑
65 2
65g x
=
x=2g,
答:生成氢气的质量是2g.
Zn+H2SO4═ZnSO4+H2↑
65 2
65g x
| 65 |
| 65g |
| 2 |
| x |
x=2g,
答:生成氢气的质量是2g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
下列有关说法正确的是( )
| A、常温下,过氧化氢溶液极易分解产生氧气 |
| B、验满氧气的方法是用带火星的木条靠近集气瓶口 |
| C、我国水资源很丰富,不需要节约用水 |
| D、因自然界各种水体均有自净能力,故污水可以任意排放 |
下列有关57号元素镧(La)的说法不正确的是( )
| A、该元素原子的质子数为57 |
| B、该元素为非金属元素 |
| C、该元素原子的核外电子数为57 |
| D、该元素原子的核电荷数为57 |
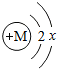 已知某粒子(原子或离子)的核外电子结构示意图如图所示.
已知某粒子(原子或离子)的核外电子结构示意图如图所示.