题目内容
 向100g 4%的氢氧化钠溶液中逐滴滴入稀硫酸,当滴入的稀硫酸与氢氧化钠恰好完全反应时,消耗稀硫酸42g.请通过计算写好标签,将最终所得溶液装瓶,贴上标签.要求写出计算过程.
向100g 4%的氢氧化钠溶液中逐滴滴入稀硫酸,当滴入的稀硫酸与氢氧化钠恰好完全反应时,消耗稀硫酸42g.请通过计算写好标签,将最终所得溶液装瓶,贴上标签.要求写出计算过程.考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:氢氧化钠与硫酸反应生成硫酸钠和水,根据恰好完全反应消耗氢氧化钠质量计算出生成的溶质硫酸钠的质量,再用硫酸钠的质量除以反应后溶液的质量即可.
解答:解:恰好完全反应时用去NaOH质量为:100g×4%=4g
设生成Na2SO4的质量为x
H2SO4+2NaOH=Na2SO4+2H2O
80 142
4g x
=
x=7.1g
所得溶液中溶质质量分数=
×100%=5%
答:所得溶液中溶质质量分数为5%.
标签为: .
.
设生成Na2SO4的质量为x
H2SO4+2NaOH=Na2SO4+2H2O
80 142
4g x
| 80 |
| 4g |
| 142 |
| x |
x=7.1g
所得溶液中溶质质量分数=
| 7.1g |
| 100g+42g |
答:所得溶液中溶质质量分数为5%.
标签为:
 .
.点评:此题是根据化学方程式计算的题目,解题的关键是根据已知量根据化学方程式对未知量进行的求解,属基础性计算考查题.

练习册系列答案
相关题目
下列实验操作中正确的是( )
A、 加热溶液 |
B、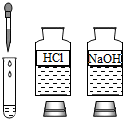 酸碱中和反应 |
C、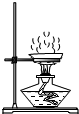 蒸发食盐水 |
D、 称量烧碱 |
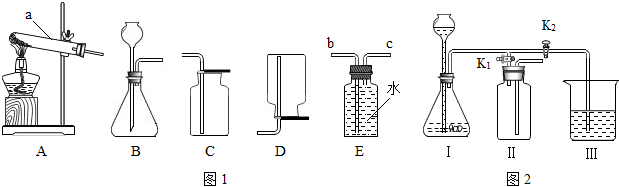
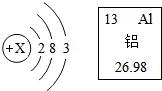 回答下列问题:
回答下列问题: