题目内容
6. 如图是某化学反应前后反应物与生成物分子及其数目变化微观示意图,其中不同的圆球代表不同的原子.下列说法正确的是( )
如图是某化学反应前后反应物与生成物分子及其数目变化微观示意图,其中不同的圆球代表不同的原子.下列说法正确的是( )| A. | 该反应属于复分解反应 | |
| B. | 参加反应的两种分子个数比不能确定 | |
| C. | 反应前后,原子的种类与数目都发生了改变 | |
| D. | 反应前后,分子的种类与数目都发生了改变 |
分析 观察化学反应前后反应物与生成物分子及其数目变化微观示意图,根据反应的特点分析反应的类型;根据微粒的变化分析分子、原子的变化及各物质反应的微粒个数关系等.
解答 解:由化学反应前后反应物与生成物分子及其数目变化微观示意图可知,各物质反应的微粒个数关系是: A、由图示可知,反应由两种物质生成了一种物质,属于化合反应,不属于复分解反应.故A错误;
A、由图示可知,反应由两种物质生成了一种物质,属于化合反应,不属于复分解反应.故A错误;
B、由上图可知,参加反应的两种分子个数比是2:1,故B错误;
C、由微粒的变化可知,反应前后,原子的种类与数目都没有改变,故C错误;
D、由微粒的变化可知,反应前后,分子的种类与数目都发生了改变.故D正确.
故选D.
点评 解答本题的关键是要充分理解图中提供的信息方面的内容,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
8.在一次化学实验中,同学们将饱和CuSO4溶液逐滴加到5mL饱和NaOH溶液中,观察到以下异常实验现象:
在实验①中同学们根据所学初中化学知识判断蓝色沉淀是Cu(OH)2,请你写出生成蓝色沉淀的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】Ⅰ.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO
Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色
【猜想与讨论】小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解.其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体(合理即可).
同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中.
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
【实验探究】为验证猜想,同学们用Cu(OH)2粉末(其它试剂可任选)设计如下实验.请你填写表中的空格.
【结论与反思】(1)根据实验,并进一步查阅资料知道,Cu(OH)2在NaOH溶液中溶解生成Na2Cu(OH)4,反应的化学方程式是Cu(OH)2+2NaOH=Na2Cu(OH)4.
(2)根据实验可知饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是资料Ⅰ显示Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色(合理即可).
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1-6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7-9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色 |
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】Ⅰ.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO
Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色
【猜想与讨论】小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解.其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体(合理即可).
同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中.
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
【实验探究】为验证猜想,同学们用Cu(OH)2粉末(其它试剂可任选)设计如下实验.请你填写表中的空格.
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 | 沉淀不消失 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加到NaOH浓溶液中,充分振荡 | 沉淀消失,溶液变成亮蓝色 | 猜想二正确 |
(2)根据实验可知饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是资料Ⅰ显示Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色(合理即可).
1.下列除去混合物中少量杂质(括号内为杂质)的方案中,不合理的是( )
| 混合物 | 思路方法 | 选用物质 | |
| A | CO (CO2) | 吸收 | 过量的氢氧化钠溶液 |
| B | CaCl2 (HCl) | 转化、过滤 | 过量的碳酸钙 |
| C | HCl(BaCl2) | 沉淀、过滤 | 适量的CuSO4溶液 |
| D | FeSO4(CuSO4) | 置换、过滤 | 过量的铁粉 |
| A. | A | B. | B | C. | C | D. | D |
11.划燃的火柴如果火焰在上直立,火柴梗不易继续燃烧其原因是( )
| A. | 温度达不到着火点 | B. | 火柴梗着火点升高 | ||
| C. | 火柴梗不是可燃物 | D. | 氧气不足 |
18.某化学兴趣小组活动小组的同学学习“灭火器原理”(如图)后,进行如下研究.
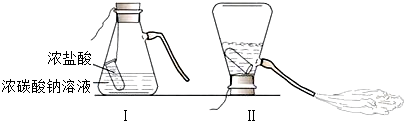
(1)锥形瓶中残留废液所含溶质是什么物质?
[猜想与假设]小华说:溶质可能是Na2CO3、NaCl和HCl;小李说:溶质可能是NaCl;小明说:溶质可能是Na2CO3和NaCl;小丽说溶质可能是:NaCl和HCl;
大家一致认为小华的猜想不正确,理由是碳酸钠和盐酸不能共存;
【初步验证】去少量试液滴加无色酚酞后不变色.
【查阅资料】溶液中氯离子遇到硝酸银溶液会产生只白色沉淀,Na2CO3溶液可使酚酞变红.
【得出结论】该溶质可能含有NaCl,或NaCl和HCl.
【进行实验】
由实验①不能(填“能”或“不能”)确定溶质一定只含有氯化钠,理由是盐酸和氯化钠溶液中都含有氯离子,遇到硝酸银溶液都会产生白色沉淀;根据实验②现象可知,小丽同学的猜想正确,写出发生反应的化学方程式CuO+2HCl=CuCl2+H2O.
(2)小华思考:锥形瓶中废液怎么处理?
【拓展与应用】根据HCl的性质,无需另加试剂,要对废液进行蒸发操作即可从废液中得到NaCl固体.

(1)锥形瓶中残留废液所含溶质是什么物质?
[猜想与假设]小华说:溶质可能是Na2CO3、NaCl和HCl;小李说:溶质可能是NaCl;小明说:溶质可能是Na2CO3和NaCl;小丽说溶质可能是:NaCl和HCl;
大家一致认为小华的猜想不正确,理由是碳酸钠和盐酸不能共存;
【初步验证】去少量试液滴加无色酚酞后不变色.
【查阅资料】溶液中氯离子遇到硝酸银溶液会产生只白色沉淀,Na2CO3溶液可使酚酞变红.
【得出结论】该溶质可能含有NaCl,或NaCl和HCl.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量废液滴加少量硝酸银溶液 | 有白色沉淀产生 |
| ② | 另取适量废液,加入少量氧化铜 | 黑色粉末逐渐溶解,溶液逐渐变成蓝色 |
(2)小华思考:锥形瓶中废液怎么处理?
【拓展与应用】根据HCl的性质,无需另加试剂,要对废液进行蒸发操作即可从废液中得到NaCl固体.
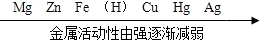 根据下面部分金属的活动性顺序回答:
根据下面部分金属的活动性顺序回答: