题目内容
下列生活中的常见物质能使无色酚酞试液变红的是( )
|
| A. | 食醋 | B. | 柠檬汁 | C. | 食盐水 | D. | 肥皂水 |
| 酸碱指示剂及其性质.. | |
| 专题: | 常见的碱 碱的通性. |
| 分析: | 无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红,据此结合常见物质的酸碱性进行分析判断. |
| 解答: | 解:A、食醋显酸性,不能使无色酚酞试液变红色,故选项错误; B、柠檬汁中含有柠檬酸,显酸性,不能使无色酚酞试液变红色,故选项错误; C、食盐水显中性,不能使无色酚酞试液变红色,故选项错误; D、肥皂水显碱性,能使无色酚酞试液变红色,故选项正确. 故选:D. |
| 点评: | 本题难度不大,掌握溶液的酸碱性和溶液pH大小之间的关系、常见物质的酸碱性是正确解题的关键. |

将36.5克稀盐酸和40克氢氧化钠溶液混合,充分反应,则所得溶液的pH值( )
|
| A. | 一定等于7 | B. | 可能等于7 | C. | 一定大于7 | D. | 一定小于7 |
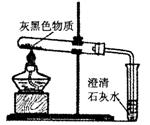
学习了金属的化学性质后,某兴趣小组进行了如下实验:将足量镁条加入到氯化铁溶液中,观察到镁条表面有气泡产生,一段时间后,有黑色固体粉末生成.
【提出问题】产生气体是什么物质?
【作出猜想】猜想一:可能是氧气;猜想二:可能是氢气;猜想三:可能是二氧化碳.
【交流讨论】大家思考后,一致认为猜想三不合理,其理由是 反应物中不含碳元素,不符合质量守恒定律 .
【实验与结论】
| 实验步骤 | 现象 | 结论 |
| ①先用试管收集该气体,再将带火星的木条伸入试管 |
| 猜想一不成立 |
| ②用尖嘴导管将气体导出并引燃,同 时在上方放一块干冷的玻璃片 | 该气体能燃烧,且玻璃片上有 出现 | 猜想二成立 |
【继续探究】用pH试纸测得氯化铁溶液pH约为2,说明氯化铁溶液中含有较多的 氢 离子.
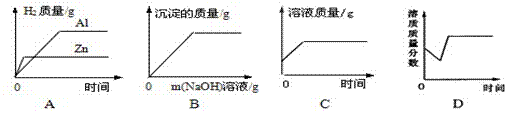
氢氧化铝是一种不溶于水的白色固体,能与稀盐酸反应,也能与氢氧化钠溶液反应.氢氧化铝与氢氧化钠溶液反应的化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.下列有关说法错误的是( )
|
| A. | 氢氧化铝属于氧化物 |
|
| B. | 在NaAlO2中铝元素的化合价为+3价 |
|
| C. | 向稀盐酸中加入氢氧化铝,发生复分解反应 |
|
| D. | 向氯化铝溶液中逐滴加入氢氧化钠溶液,先产生白色沉淀,后来白色沉淀又消失 |
物质X是一种可再生绿色能源,其燃烧的化学方程式为X+3O2 2CO2+3H2O,则X的化学式为( )
2CO2+3H2O,则X的化学式为( )
|
| A. | C2H4 | B. | CH3OH | C. | C2H5OH | D. | C2H6 |
 认为可能是Mg0
认为可能是Mg0 :乙同学认为可能是Mg2(OH)2CO3;丙同学认为可能是Mg(OH)2。
:乙同学认为可能是Mg2(OH)2CO3;丙同学认为可能是Mg(OH)2。 C.+3
C.+3  D.+4
D.+4