题目内容
【题目】金属材料为人类的进步和发展作出了巨大的贡献。
(1)钛和钛合金是制造火箭、导弹、航天飞机的重要材料。主要利用了它们具有_____(填字母)等性能。
A 熔点高、密度小、机械性能好
B 熔点低、硬度大、韧性好
C 密度大、耐磨、耐腐蚀
(2)用盐酸除去自行车钢圈上的铁锈,其反应的化学方程式是_____。
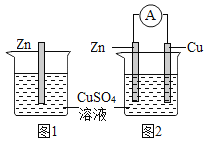
(3)现有形状大小完全相同的铝片、铜片和铁片,从下列药品中选一种来验证三者的活动性顺序,一定不能够选择的是_____(填序号,可多步实验)。
①稀硫酸
②硫酸铝溶液
③硫酸铜溶液
④硫酸亚铁溶液
【答案】A ![]() ②
②
【解析】
(1)钛和钛合金是制造火箭、导弹、航天飞机的重要材料,因为它们熔点高、密度小、机械性能好,故选A;
(2)铁锈的主要成分是氧化铁,盐酸和氧化铁反应生成氯化铁和水,化学方程式为:![]() ;
;
(3)形状大小完全相同的铝片、铜片和铁片,分别加入等量的稀硫酸中,产生气泡速率较快的是铝,产生气泡速率较慢的是铁,不产生气泡的是铜,所以金属活动性:铝>铁>铜;①正确;形状大小完全相同的铝片、铜片和铁片,分别加入等量的硫酸铝溶液中,三者均不反应,无法验证金属活动性,②错误;形状大小完全相同的铝片、铜片和铁片,先将铁片加入硫酸铜溶液中,一段时间后铁片表面有红色固体析出,说明铁的金属活动性强于铜,将铁片取出,再加入铝片,一段时间后铝片表面有银白色固体析出,说明铝的金属活动性强于铁,③正确;形状大小完全相同的铝片、铜片和铁片,将铜片加入硫酸亚铁溶液中,不反应,说明铜的金属活动性弱于铁,将铜片取出,再加入铝片,一段时间后铝片表面有银白色固体析出,说明铝的金属活动性强于铁,④正确;故选②。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案【题目】下列除杂所选用试制与操作方法均正确的是
选项 | 物质 | 除杂试剂及操作 |
A |
| 加水溶解、过滤、蒸发结晶 |
B |
| 加入过量稀盐酸,蒸发结晶 |
C |
| 加入过量 |
D |
| 通入灼热的CuO |
A.AB.BC.CD.D
【题目】实验课上,老师知道某兴趣小组进行粗盐提纯的实验,邀请你帮助他们完成下面的实验报告。
(实验名称)粗盐的提纯
(查阅资料)
(1)粗盐中含有泥沙及少量可溶性MgCl2、CaCl2、Na2SO4等杂质。
(2)Ba(OH)2是一种易溶于水的强碱。
(主要玻璃仪器)量筒、烧杯、漏斗、玻璃棒、胶头滴管、酒精灯
(主要试剂)粗盐样品、稀盐酸、BaCl2溶液,NaOH溶液,Na2CO3溶液,蒸馏水
(实验过程)
步骤及目的 | 过程及说明 |
一、去除粗盐中的泥沙 | 1.称取粗盐样品10.0g,用蒸馏水充分溶解 2.过滤去除泥沙的溶液I 以上两步操作中均需要使用到玻璃棒,玻璃棒的作用分别是:溶解时:_______;过滤时:_______。 |
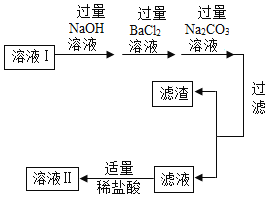
二、去除可溶 性杂质 | 将溶液I按如图流程图进行处理: 1. 加入“过量NaOH溶液时”,发生反应的化学方程式是_________。 2. 加入“过量碳酸钠溶液”发生反应的方程式是________。 3. 过滤后,所得的滤渣成分有_______种。 4. 判断“稀盐酸适量”的方法是_______________。
|
三、获得产品 | 将溶液Ⅱ注入_______(填仪器名称)中,蒸发结晶,观察到_______,停止加热,利用余热蒸干。装置完全冷却后,获得干燥的产品9.4g。 |
四、数据处理 | 该粗盐样品中氯化钠的质量分数是94% |
(结果与反思)
(1)实验操作、试剂和装置均不存在问题,老师却指出该样品中氯化钠的质量分数不是94%,原因是________________。
(2)小明提出,如果步骤二中只调换“过量的NaOH溶液”与“过量的BaCl2溶液”的加入顺序,对除杂结果也不会产生影响,你_______(填“同意”或“不同意”)小明的观点。