题目内容
(6分)某校兴趣小组对氢氧化钠溶液与稀盐酸混合后的有关问题,进行了如下探究,请同学们一起参与此次探究之旅。
(1)探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
【方案设计】小丽、小林两位同学设计了如下方案进行探究:
方案设计者 | 方案步骤 | 方案预估现象 | 方案预估结论 |
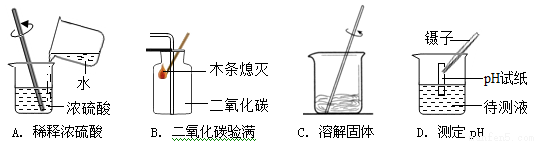
小丽 | 用一根洁净的玻璃棒蘸取反应后的溶液沾在pH试纸上,把试纸呈现的颜色与标准比色卡对照 | pH=7 | 恰好完全中和 |
小林 | 取少量反应后的溶液于一支试管中,并向试管中滴加稀硝酸和硝酸银溶液 | 有白色沉淀生产 | 盐酸过量,没有完全中和 |
【方案评价】请判断以上设计的两个方案中, 同学的方案是正确的。
【方案反思】请分析另一个方案错误的原因: 。
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】小亮猜想:溶质有NaCl、HCl、NaOH
小丽猜想:溶质只有NaCl
小林猜想:溶质有NaCl、HCl
你的猜想:溶质有 (填化学式)
小丽认为小亮的猜想是错误的,她的理由是 。
【实验设计及验证】请你将下列实验报告填写完整:
实验操作 | 实验现象 | 实验结论 |
取反应后的溶液于试管中,加入碳酸钠溶液 | 小林猜想正确 | |
有蓝色沉淀生成 | 你的猜想正确 |
【方案评价】小丽
【方案反思】氯化钠也能和硝酸银溶液反应生成白色沉淀(其他合理答案也可)
【作出猜想】NaCl 、NaOH; HCl与NaOH能反应,不能共存
【实验设计及验证】有气泡产生
【解析】
试题分析:分析另一个方案错误的原因氯化钠也能和硝酸银溶液反应生成白色沉淀,造成了对物质鉴别的干扰,小丽认为溶质有NaCl、HCl、NaOH是不对的,因为HCl与NaOH能反应,不能共存,取反应后的溶液于试管中,加入碳酸钠溶液,有气泡冒出,说明溶质有NaCl、HCl。
考点:酸碱盐的性质和变化

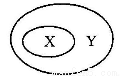
下图中的X、Y的关系为Y包含X,下列选项中符合图中关系的是
A | B | C | D | |
X | 金属 | 溶液 | 纯净物 | 化石燃料 |
Y | 单质 | 乳浊液 | 化合物 | 石油 |
(3分)测得生活中一些液体的pH如下表:
液体 | 雨水 | 糖水 | 厨房清洁剂 | 厕所清洁剂 |
pH | 5.6 | 7 | 11.8 | 2 |
(1)上述液体中,呈中性的是 ;
(2)正常雨水的pH约为5.6的原因是 ;
(3)用pH试纸测定厕所清洁剂的pH时,先将pH试纸用水润湿,结果会 (填“偏大”、“偏小”或“无影响”)。
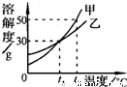
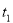 ℃时,甲和乙的溶解度相等
℃时,甲和乙的溶解度相等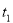 ℃时,30g乙加到100g水中形成饱和溶液
℃时,30g乙加到100g水中形成饱和溶液