题目内容
20.“绿色化学”是21世纪化学发展的主导方向,它要求从根本上消除污染,是一门彻底阻止污染物产生的科学.它包括“原料的绿色化”“化学反应的绿色化”“产物的绿色化”等内容,其中“化学反应的绿色化”要求原料物质中所有的原子完全被利用且全部转化期望的产品中.下列符合“化学反应的绿色化”的是( )
| A. | 锌粒跟稀硫酸反应制取氢气 | B. | NH3+CO2+H2O═NH4HCO3 | ||
| C. | 实验室制取二氧化碳 | D. | 电解氯化镁制取金属镁 |
分析 根据绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染;反应物的原子全部转化为期望的最终产物进行分析解答本题.
解答 解:根据绿色化学的核心和题中“化学反应的绿色化”要求原料物质中所有的原子完全被利用且全部转入期望的产品中,选项A,C,D化学反应都有不同的反应产物,只有选项B反应物的原子全部转化为期望的最终产物,符合“化学反应绿色化”.
故选B.
点评 本题考查学生根据绿色化学的核心进行分析解题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列物质属于溶液的是( )
| A. | 牛奶 | B. | 硫酸 | ||
| C. | 酒精 | D. | 碘溶解在汽油里面 |
8.做馒头时在发酵的面团中加入某种物质,既能除去面团中的酸又能使馒头变软,则加入的这种物质为( )
| A. | 氢氧化钠 | B. | 碳酸钠 | C. | 氧化钙 | D. | 氯化钠 |
15.下列广告语中,你认为不科学的是( )
| A. | 食用含碘食盐可预防甲状腺肿大 | |
| B. | 使用含氟牙膏可预防龋齿 | |
| C. | 某口服液含有丰富的氮、锌、铁等微量元素 | |
| D. | 经卫生部门检验合格的矿泉水中含少量对人人体有益的矿物质,是一种健康饮料 |
12.下列仪器可以用来直接加热的是( )
| A. | 烧瓶 | B. | 酒精灯 | C. | 蒸发皿 | D. | 量筒 |
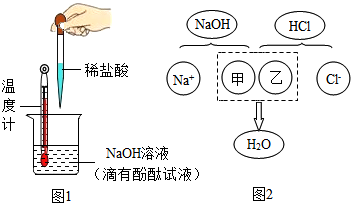
9.酸溶液和碱溶液混合会发生怎样的变化呢?某班级同学开展如图1所示相关的实验.下面是两个小组的实验
记录与分析.请根据要求回答问题:
(1)甲组同学往一定体积10%的氢氧化钠溶液样品中滴加10%的盐酸(室温下),反应中溶液温度的变化记录如下:
根据上表数据分析:
①当加入盐酸体积为10mL时,表明NaOH与HCl恰好完全反应.此判断的依据是中和反应放热,恰好完全反应时放出热量最多.
②当加入6mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和氯化钠和氢氧化钠.
③教材指出:酸与碱中和反应的结果是酸和碱各自的特性都消失.图2描述的是氢氧化钠与盐酸反应的微观实质,请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
(2)请你参与完成乙组同学的实验记录与分析.
记录与分析.请根据要求回答问题:

(1)甲组同学往一定体积10%的氢氧化钠溶液样品中滴加10%的盐酸(室温下),反应中溶液温度的变化记录如下:
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度上升 (△t)/℃ | 5.6 | 9.8 | 12.1 | 16.3 | 18.5 | 17.1 | 15.2 | 14.6 | 13.5 | 12.6 |
①当加入盐酸体积为10mL时,表明NaOH与HCl恰好完全反应.此判断的依据是中和反应放热,恰好完全反应时放出热量最多.
②当加入6mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和氯化钠和氢氧化钠.
③教材指出:酸与碱中和反应的结果是酸和碱各自的特性都消失.图2描述的是氢氧化钠与盐酸反应的微观实质,请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
(2)请你参与完成乙组同学的实验记录与分析.
| 实验操作 | 实验现象 | 分析与结论 |
| 步骤一:往装有氢氧化钠溶液样品的试管中先滴加2~3滴的 酚酞试液,再逐滴加入稀盐酸 | 现象一:有气泡产生 现象二:溶液由红色逐渐变成无色 | 1.该氢氧化钠溶液样品已变质 2.溶液碱性消失 |
| 步骤二:取步骤一反应后的溶液,然后逐滴加入该氢氧化钠溶液样品 | 现象一:有气泡产生 现象二:溶液开始不变色,后逐渐变成红色 | 1.产生“气泡”这一现象对应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑ 2.所取的步骤一反应后的溶液pH<7(填“<”、“=”或“>”) |
16.下列说法正确的是( )
| A. | 加入催化剂,化学反应一定加快 | |
| B. | 不使用催化剂,化学反应不能进行 | |
| C. | 使用催化剂,可以增加生成物的质量 | |
| D. | 使用催化剂,可以改变化学反应的速率 |