题目内容
19.甲乙两烧杯盛有相同体积、相同浓度的硫酸溶液,分别放入等质量的铝和锌,充分反应后,甲烧杯中的铝有剩余,乙烧杯中的锌全部完全反应.下列结论中正确的是( )①甲产生的氢气多②乙产生的氢气多③甲乙产生的氢气一样多.
| A. | ① | B. | ② | C. | ②③ | D. | ①③ |
分析 因为甲烧杯中铝有剩余,说明稀硫酸已用完,在此反应中产生了足够多的氢气;而乙烧杯中锌已全部反应,说明在此反应中有两种情况可能存在:①稀硫酸已用完,产生了足够的氢气,那么甲乙两烧杯中产生的氢气一样多;②稀硫酸没有全部反应,因此,就没有产生足够的氢气,在此实验中甲烧杯中产生的氢气多.
解答 解:①如果乙烧杯中稀硫酸没有全部反应,因此,就没有产生足够的氢气,在此实验中甲烧杯中产生的氢气多,故正确
②乙烧杯中产生的氢气最多与烧杯中产生的氢气一样多,故错误;
③如果乙烧杯中稀硫酸已用完,产生了足够的氢气,那么甲乙两烧杯中产生的氢气一样多,故正确.
故选:D.
点评 本题主要考查学生对完全反应和不完全反应的概念的区别,以及运用知识进行推断的能力.学生需全面分析,才能正确选择.

练习册系列答案
相关题目
4.下列物质在空气中燃烧,主要现象描述错误的是( )
| A. | 红磷燃烧产生大量白烟 | B. | 甲烷燃烧产生蓝色火焰 | ||
| C. | 硫燃烧产生蓝紫色火焰 | D. | 氢气燃烧产生淡蓝色火焰 |
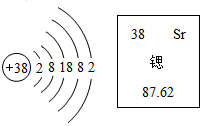
8.在化学反应中铁原子容易失去2个或3个电子,因此铁元素在化合物中常显+2价或+3价.在化合物Fe(FeO2)2中,括号前和括号内铁元素的化合价分别是( )
| A. | +2、+2 | B. | +3、+3 | C. | +3、+2 | D. | +2、+3 |
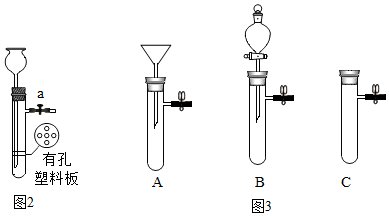
9.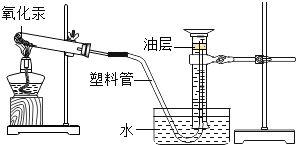 如图是研究性学习课题《化学反应中质量守恒的研究》的实验装置.本实验通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.已知:氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑
如图是研究性学习课题《化学反应中质量守恒的研究》的实验装置.本实验通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.已知:氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑
请回答下列问题:
(1)在量筒中加入一层植物油,目的是防止氧气溶于水.
(2)小明重复做四次实验,记录了“反应前、后试管及其中固体总质量”的数据,如下表,其中有明显错误的两组数据是第1次、第4次(填序号).
实验过程中还需要测量一个数据(单位:升)并作记录,则需测的数据应是氧气的体积.
(3)在每次实验中,量筒里获得物质的质量与预测结果(即理论值)不符.下列各项解释中,你认为合理的是BC(填序号).
A.该反应不遵守质量守恒定律.
B.反应结束后量筒内液面读数方法不规范
C.塑料管口放出连续均匀的气泡后才能收集气体
D.氧化汞没有完全分解就停止加热
E.该反应前后原子的种类、数目变少.
 如图是研究性学习课题《化学反应中质量守恒的研究》的实验装置.本实验通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.已知:氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑
如图是研究性学习课题《化学反应中质量守恒的研究》的实验装置.本实验通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.已知:氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑请回答下列问题:
(1)在量筒中加入一层植物油,目的是防止氧气溶于水.
(2)小明重复做四次实验,记录了“反应前、后试管及其中固体总质量”的数据,如下表,其中有明显错误的两组数据是第1次、第4次(填序号).
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 反应前试管及其中固体总质量(克) | 8.5 | 8.2 | 8.4 | 8.6 |
| 反应结束冷却后试管及其中固体总质量(克) | 8.5 | 7.8 | 8.1 | 8.8 |
(3)在每次实验中,量筒里获得物质的质量与预测结果(即理论值)不符.下列各项解释中,你认为合理的是BC(填序号).
A.该反应不遵守质量守恒定律.
B.反应结束后量筒内液面读数方法不规范
C.塑料管口放出连续均匀的气泡后才能收集气体
D.氧化汞没有完全分解就停止加热
E.该反应前后原子的种类、数目变少.