题目内容
某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入少量的稀盐酸,无气泡产生,则下列有关说法正确的是( )
| A、滤出的固体中一定只含银 |
| B、滤出的固体中一定含有银和铜,一定不含铁 |
| C、滤液中一定含有硝酸亚铁,可能含有硝酸银和硝酸铜 |
| D、滤液中一定含有硝酸亚铁,一定没有硝酸银 |
考点:金属的化学性质
专题:金属与金属材料
分析:在金属活动性顺序中,铁排在铜和银的前边,可以和硝酸银及硝酸铜溶液反应,生成银和铜以及硝酸亚铁,向滤渣中加入少量的稀盐酸,无气泡产生,说明滤液中没有硝酸银.
解答:解:由题意可知,在金属活动性顺序中,铁排在铜和银的前边,可以和硝酸银及硝酸铜溶液反应,生成银和铜以及硝酸亚铁.向滤渣中加入少量的稀盐酸,无气泡产生,说明滤渣中一定没有铁、一定有银、可能有铜.滤液中一定有硝酸亚铁.可能含有硝酸银、硝酸铜,由以上分析可知:
A、滤出的固体中一定含有银,可能有铜.A错误;
B、滤出的固体中一定含有银,一定不含铁,可能含有铜,B错误;
C、滤液中一定有硝酸亚铁,可能含有硝酸银、硝酸铜.C正确;
D、滤液中一定有硝酸亚铁,可能含有硝酸银、硝酸铜.D错误.
故选:C.
A、滤出的固体中一定含有银,可能有铜.A错误;
B、滤出的固体中一定含有银,一定不含铁,可能含有铜,B错误;
C、滤液中一定有硝酸亚铁,可能含有硝酸银、硝酸铜.C正确;
D、滤液中一定有硝酸亚铁,可能含有硝酸银、硝酸铜.D错误.
故选:C.
点评:本题考查的金属与混合盐溶液的反应,完成此题,可以依据金属活动性顺序以及题干提供的信息进行.所以要求同学们在平时的学习中加强基础知识的记忆,以便能够灵活应用.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
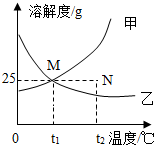 如图为甲、乙两种固体物质在水中的溶解度曲线,下列说法错误的是( )
如图为甲、乙两种固体物质在水中的溶解度曲线,下列说法错误的是( )| A、升高温度能使乙物质的不饱和溶液变成饱和溶液 |
| B、在t1℃时,M点表示甲、乙两物质的溶解度相等 |
| C、在t2℃时,N点表示甲物质的不饱和溶液 |
| D、在t1℃时,100g溶液中可以溶解25g甲物质 |
下列实验方法错误的是( )
| A、用肥皂水区别硬水和软水 |
| B、用带火星的木条区别空气和O2 |
| C、用水区别NH4NO3和固体NaOH 两种固体 |
| D、用湿润的红色石蕊试纸区别CO和CO2 |
下列图象能正确反映所对应叙述关系的是( )
A、 向NaOH溶液中不断加水 |
B、 向饱和的硝酸钾溶液中加入硝酸钾固体 |
C、 向H2SO4和CuSO4混合液中滴加NaOH溶液 |
D、 煅烧一定质量的石灰石 |
下列仪器不能在酒精灯上加热的是( )
| A、烧杯 | B、量筒 |
| C、蒸发皿 | D、燃烧匙 |

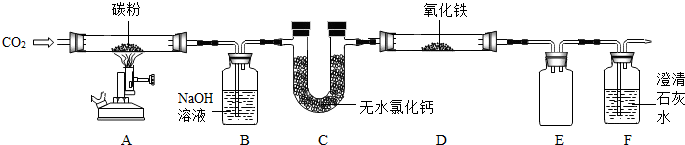
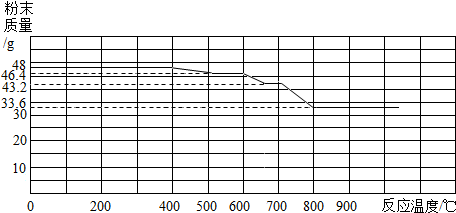

 某校化学小组同学从家中带来淀粉、食盐、纯碱、泡打粉、去污粉和部分变质的熟石灰6种固体物质.老师从中取出任意3种并编号,让小组同学通过实验确认分别为哪种固体.
某校化学小组同学从家中带来淀粉、食盐、纯碱、泡打粉、去污粉和部分变质的熟石灰6种固体物质.老师从中取出任意3种并编号,让小组同学通过实验确认分别为哪种固体.