题目内容
5.某研究小组对用H2O2分解产生H2O和O2 的实验条件进行探究,他们进行了以下实验:①向盛有5mL5%的H2O2溶液的试管中,伸入带火星的木条,木条不复燃.②向盛有5mLA%的H2O2溶液的试管中,加入agMnO2,伸入带火星的木条,木条复燃.③向盛有5mLA%的H2O2溶液的试管中,加入agFe2O3,伸入带火星的木条,木条复燃.④经检验,②、③中反应后试管中仍分别含有agMnO2 和agFe2O3.(1)实验②、③中H2O2溶液的浓度A%以5%为宜.MnO2 和Fe2O3在上述反应中的作用催化作用,写出③中的反应方程式2H2O2$\frac{\underline{\;Fe_{2}O_{3}\;}}{\;}$2H2O+O2↑,该反应属于分解反应.(填反应类型)
(2)研究小组还对溶液的浓度、催化剂的种类等实验条件对反应速率的影响进行了探究.下表选取了部分实验数据:用足量等体积的H2O2溶液制取相同体积的O2所需的时间.
| 浓度 时间 条件 | 30%的H2O2溶液 | 15%的H2O2溶液 | 5%的H2O2溶液 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
分析 (1)有①②③对比可知加入二氧化锰、氧化铁都使反应速度迅速提高,且由④可知其质量没有改变,可说明它是催化剂;此题是证明催化剂的催化作用,故应该创设相同的其他条件很有必要;
(2)从图表数据可以看出过氧化氢相同时,比较不同的催化剂,催化剂相同时可证明溶液浓度与反应速度的关系.
解答 解:(1)有①②③对比可知加入二氧化锰、氧化铁后的反应速度明显提高,且由④可知其质量没有改变,故可说明它是这一反应的催化剂;②③是创设相同的条件只改变加入的物质进行对比实验,在过氧化氢溶液的溶质质量分数和体积都相同的条件下实验,才能比较出不加催化剂和加入二氧化锰或氧化铁后的催化作用;③是氧化铁做催化剂,过氧化氢分解产生水和氧气,反应的方程式为:2H2O2$\frac{\underline{\;Fe_{2}O_{3}\;}}{\;}$2H2O+O2↑; 该反应是一种物质生成两种物质的分解反应;
故答案为:5%;催化作用; 2H2O2$\frac{\underline{\;Fe_{2}O_{3}\;}}{\;}$2H2O+O2↑; 分解;
(2)?从图表数据可以看出过氧化氢相同时,催化剂的效果不同;催化剂相同时可证明溶液浓度越大,反应速度越快;
故答案为:①相同条件下,MnO2的催化效果比Fe2O3好;②在其他条件相同的情况下,H2O2浓度越大,产生氧气的速度越快.
点评 此题考查了过氧化氢制取氧气时不同催化剂的效果,以及反应物的浓度与反应速度的关系,也培养了学生分析图表,对比实验的能力.

练习册系列答案
相关题目
13.人呼出的气体中的主要成分是( )
| A. | 水蒸气 | B. | 二氧化碳 | ||
| C. | 二氧化碳、水和氮气 | D. | 氧气 |
14.下列化合物中,氮元素的化合价由低到高排列的是( )
| A. | NO NO2 NH3 HNO3 | B. | NO NH3NO2HNO3 | ||
| C. | NH3 NO NO2 HNO3 | D. | HNO3NO2NH3NO |
15.如图所示变化属于化学变化的是( )
| A. |  对玻璃片呼气 | B. |  蜡烛燃烧 | C. |  灯泡通电发光 | D. |  湿衣晾干 |
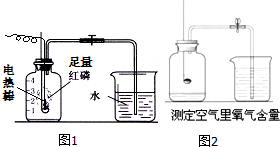 按图1组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:
按图1组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题: