题目内容
16.下列图象能正确反映对应变化关系的是( )| A. | 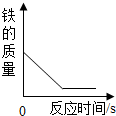 过量铁粉测定空气中氧气含量 | |
| B. |  往等质量的HCl溶液中分别加入Na2CO3和NaHCO3固体 | |
| C. | 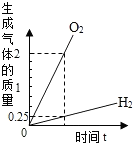 将水通电电解一段时间 | |
| D. | 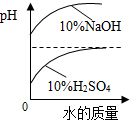 稀释10%的NaOH和10% 的H2SO4中pH变化 |
分析 A、根据铁在空气中不燃烧解答;
B、根据碳酸氢钠和碳酸钠与稀盐酸反应的化学方程式可以完成解答;
C、根据电解水得到的氧气和氢气的质量比解答;
D、根据酸加水稀释pH值升高,碱加水稀释pH值降低解答.
解答 解:
A、铁在空气中不燃烧,铁的质量不变,故错误;
B、NaHCO3+2HCl═NaCl+H2O+CO2↑
84 73 44
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
所以往等质量的HCl溶液中分别加入Na2CO3和NaHCO3固体产生二氧化碳的质量相等,故错误;
C、电解水得到的氧气和氢气的质量比是8:1,图示中是2g:0.25g=8:1,故正确;
D、酸加水稀释pH值升高但不能到7,碱加水稀释pH值降低,但不能降到7,故错误;
故选C.
点评 解答这类题目时,首先,要知道酸碱加水稀释后pH值的变化情况,一定要理解催化剂的概念、催化作用,知道金属与酸反应产生氢气多少的判断方法,根据所给的问题情景及相关信息,结合所学的相关知识和技能,联系起来细心地探究、推理后,按照题目要求进行选择或解答即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.实验室用一定质量的氯酸钾和二氧化锰的混合物加热制取氧气,反应前后二氧化锰在固体混合物中的质量分数( )
| A. | 变小 | B. | 变大 | C. | 不变 | D. | 不能判断 |
11.2013年12月山东出现了一起夺命快递事件,原因就是吸入了包装泄漏的氟乙酸甲酯,氟乙酸甲酯化学式为C3H5FO2,下列说法错误的是( )
| A. | 氟乙酸甲酯是有机物 | B. | 氟乙酸甲酯中碳元素的含量最高 | ||
| C. | 氟乙酸甲酯含有11个原子 | D. | 氟乙酸甲酯由四种元素组成 |
1.某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
【产品与原理】该厂采用“侯氏制碱法”生产化工产品--纯碱(Na2CO3)和化肥NH4Cl.生产原理是:将NH3和CO2通入饱和食盐水中得到NaHCO3和NH4Cl的混合物,反应为:NaCl(饱和)+NH3+CO2+H2O═NaHCO3↓+NH4Cl;分离出NaHCO3,加热制得纯碱.
【生产流程】

【相关资料】(1)NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+HCl↑
(2)已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
【问题讨论】:
(1)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通入二氧化碳气体,溶液中会有碳酸氢钠晶体析出.试分析该流程需要加压条件的原因是:增大CO2的溶解度.
(2)反应①中发生了两个反应,写出中和化学方程式:NaOH+HCl═NaCl+H2O_.
(3)溶液B中的溶质有NaHCO3、NaCl、NH4Cl、NH4HCO3四种中的任意两种(至少写出两种).
(4)上述生产流程中可循环使用的是A、B(填序号).
A.挥发性气体C B.溶液D C.氢氧化镁 D.化肥NH4Cl
(5)在氨碱工业处理剩余的氯化铵溶液时,为何不直接蒸发结晶析出氯化铵固体?答:氯化铵受热易分解.
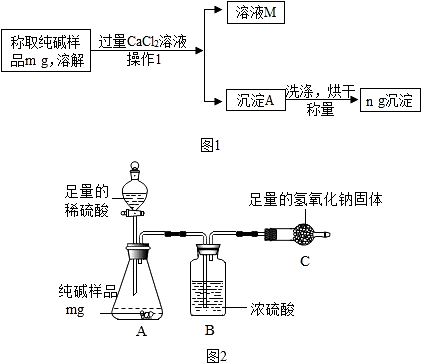
(6)“侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠,某化学兴趣小组的同学拟测定某纯碱样品中Na2CO3的质量分数,通过下图1和图2两种方案分别测定,你认为图2方案更易产生误差,原因C装置中氢氧化钠会吸收空气中二氧化碳和水.
【产品与原理】该厂采用“侯氏制碱法”生产化工产品--纯碱(Na2CO3)和化肥NH4Cl.生产原理是:将NH3和CO2通入饱和食盐水中得到NaHCO3和NH4Cl的混合物,反应为:NaCl(饱和)+NH3+CO2+H2O═NaHCO3↓+NH4Cl;分离出NaHCO3,加热制得纯碱.
【生产流程】

【相关资料】(1)NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+HCl↑
(2)已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
(1)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通入二氧化碳气体,溶液中会有碳酸氢钠晶体析出.试分析该流程需要加压条件的原因是:增大CO2的溶解度.
(2)反应①中发生了两个反应,写出中和化学方程式:NaOH+HCl═NaCl+H2O_.
(3)溶液B中的溶质有NaHCO3、NaCl、NH4Cl、NH4HCO3四种中的任意两种(至少写出两种).
(4)上述生产流程中可循环使用的是A、B(填序号).
A.挥发性气体C B.溶液D C.氢氧化镁 D.化肥NH4Cl
(5)在氨碱工业处理剩余的氯化铵溶液时,为何不直接蒸发结晶析出氯化铵固体?答:氯化铵受热易分解.
(6)“侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠,某化学兴趣小组的同学拟测定某纯碱样品中Na2CO3的质量分数,通过下图1和图2两种方案分别测定,你认为图2方案更易产生误差,原因C装置中氢氧化钠会吸收空气中二氧化碳和水.

5.通过下列化学反应不能达到目的是( )
| A. | 制氯化铁:2Fe+3CuCl2=2FeCl3+3Cu | |
| B. | 用稀硫酸除去炭粉中的少量氧化铜:CuO+H2SO4=CuSO4+H2O | |
| C. | 用硝酸钡溶液区别氢氧化钠溶液和硫酸钾溶液:K2SO4+Ba(NO3)2=BaSO4↓+2KNO3 | |
| D. | 用碳酸氢钠治疗胃酸过多症:NaHCO3+HCl=NaCl+H2O+CO2↑ |
6.下列说法不正确的是( )
| A. | 人体缺铁会引起贫血 | |
| B. | 老年人缺钙会发生骨质疏松、容易骨折 | |
| C. | 人体缺乏维生素A会引起坏血病 | |
| D. | 人体摄入的微量元素不能太多 |
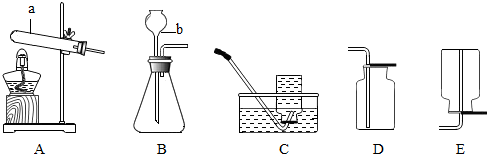
 (1)写出带有标号的仪器名称
(1)写出带有标号的仪器名称