题目内容
2.根据物质的质量分数,判断下列物质可能是纯净物的是( )| A. | 含氮33%的硝酸铵(NH4NO3) | B. | 氧的质量分数为20%的氧化铜 | ||
| C. | 氢的质量分数为10%的水 | D. | 含钙45%的碳酸钙 |
分析 纯净物由一种物质组成,混合物由两种或两种以上的物质组成.
解答 解:A、硝酸铵中氮元素质量分数是35%,因此含氮33%的硝酸铵是混合物;
B、氧化铜的相对分子质量是80,氧原子的相对原子质量是16,氧化铜中氧元素的质量分数是20%,因此含氧20%的氧化铜可能是纯净物;
C、水中氢元素的质量分数为11.1%,因此含氢元素10%的水不是纯净物;
D、碳酸钙中钙元素的质量分数是40%,因此含钙元素45%的碳酸钙不是纯净物.
故选:B.
点评 本题主要考查元素质量分数方面的问题,要根据计算判断各种说法的正误.

练习册系列答案
相关题目
3.小玲通过查阅资料知道了牙膏的主要成分.她将一定比例的碳酸钙粉末和食盐倒入小烧杯中,然后加入适量的甘油(保湿剂0、甜味剂和香精等,搅拌均匀后制得牙膏.
(1)牙膏是混合物(填纯净物、混合物)
(2)小远测定自制牙膏及其他清洁用品的pH,记录如表:
厕洁灵显碱性(填酸性、碱性、中性),油污净能使酚酞试液变成红色.
(3)牙膏中的碳酸钙粉末作摩擦剂,提高洁齿效果.这种碳酸钙是将二氧化碳通入石灰浆制得的,请写出以石灰石和水为原料制取这种碳酸钙的化学方程式:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
(4)从石灰石中提纯碳酸钙根本的原理都是先使不溶性物质转化为可溶性物质,再通过一定的方法重新得到纯净的碳酸钙.除(3)中转化途径外,还可以写出另外的途径:
石灰石 $\stackrel{①}{→}$-$\stackrel{②}{→}$碳酸钙写出符合条件的化学方程式①CaCO3+2HCl═CaCl2+H2O+CO2↑;②Na2CO3+CaCl2=CaCO3↓+2NaCl.
(1)牙膏是混合物(填纯净物、混合物)
(2)小远测定自制牙膏及其他清洁用品的pH,记录如表:
| 物质 | 自制牙膏 | 洁厕灵 | 油污净 |
| pH | 8 | 2 | 12 |
(3)牙膏中的碳酸钙粉末作摩擦剂,提高洁齿效果.这种碳酸钙是将二氧化碳通入石灰浆制得的,请写出以石灰石和水为原料制取这种碳酸钙的化学方程式:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
(4)从石灰石中提纯碳酸钙根本的原理都是先使不溶性物质转化为可溶性物质,再通过一定的方法重新得到纯净的碳酸钙.除(3)中转化途径外,还可以写出另外的途径:
石灰石 $\stackrel{①}{→}$-$\stackrel{②}{→}$碳酸钙写出符合条件的化学方程式①CaCO3+2HCl═CaCl2+H2O+CO2↑;②Na2CO3+CaCl2=CaCO3↓+2NaCl.
7.对于下列几种化学符号,有关说法正确的是( )
①N ②Na+ ③ ④P2O5 ⑤KClO3.
④P2O5 ⑤KClO3.
①N ②Na+ ③
 ④P2O5 ⑤KClO3.
④P2O5 ⑤KClO3.| A. | 表示物质组成的化学式有①④⑤ | |
| B. | 表示阳离子的有②③ | |
| C. | ④中数字“5”表示五氧化二磷中有5个氧原子 | |
| D. | ⑤中氯元素的化学价为+3 |
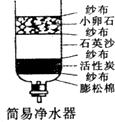 如图是小冬同学制作的简易净水器:
如图是小冬同学制作的简易净水器: