题目内容
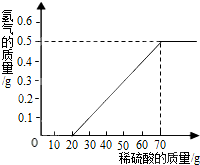 某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应,测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).
某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应,测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).(1)当稀硫酸的质量为70g,产生的氢气的质量为
(2)用化学方程式说明当稀硫酸的质量不多于20g时,不产生氢气的原因:
(3)计算镁条中氧化镁的质量分数(写出计算过程).
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据产生氢气的质量与稀硫酸的质量关系图,读出产生氢气的质量;
(2)镁条的表面有氧化镁能与稀硫酸反应;
(3)根据镁与稀硫酸反应的方程式求出镁的质量,再计算镁条中氧化镁的质量分数.
(2)镁条的表面有氧化镁能与稀硫酸反应;
(3)根据镁与稀硫酸反应的方程式求出镁的质量,再计算镁条中氧化镁的质量分数.
解答:解:
(1)由产生氢气的质量与稀硫酸的质量关系图可知,当稀硫酸的质量为70g,产生的氢气的质量为0.5g;
(2)由于镁易于空气中的氧气反应在镁条的表面生成了氧化镁,稀硫酸首先与镁条表面的氧化镁薄膜发生了反应,所以不产生氢气,故反应的方程式是:MgO+H2SO4=MgSO4+H2O.
(3)设镁的质量为x
Mg+H2SO4=MgSO4+H2↑
24 2
x 0.5g
=
x=6g
镁条中氧化镁的质量分数
×100%=40%
答案:
(1)0.5
(2)MgO+H2SO4=MgSO4+H2O;
(3)镁条中氧化镁的质量分数40%
(1)由产生氢气的质量与稀硫酸的质量关系图可知,当稀硫酸的质量为70g,产生的氢气的质量为0.5g;
(2)由于镁易于空气中的氧气反应在镁条的表面生成了氧化镁,稀硫酸首先与镁条表面的氧化镁薄膜发生了反应,所以不产生氢气,故反应的方程式是:MgO+H2SO4=MgSO4+H2O.
(3)设镁的质量为x
Mg+H2SO4=MgSO4+H2↑
24 2
x 0.5g
| 24 |
| 2 |
| x |
| 0.5g |
x=6g
镁条中氧化镁的质量分数
| 10g-6g |
| 10g |
答案:
(1)0.5
(2)MgO+H2SO4=MgSO4+H2O;
(3)镁条中氧化镁的质量分数40%
点评:较活泼的金属易于空气中的氧气反应,在金属的表面形成了金属氧化物,当与酸反应时首先金属表面的氧化物与酸反应不能放出氢气.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
我国曾发生过多次将工业用盐如亚硝酸钠(NaNO2)误作食盐用于烹饪而引起的中毒事件,下列说法正确的是( )
| A、亚硝酸钠中N的化合价为+3 |
| B、亚硝酸钠中Na、N、O的原子个数比为23:14:32 |
| C、亚硝酸钠中含有一个氧分子 |
| D、亚硝酸钠是有机物 |
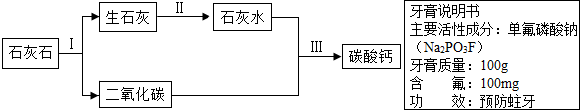
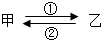 甲、乙是初中化学常见的物质,它们在一定条件下能如图所示相互转化.
甲、乙是初中化学常见的物质,它们在一定条件下能如图所示相互转化.