题目内容
13.某溶液中仅含有AgNO3、Cu(NO3)2两种溶质,某课外小组的同学将溶液分为A、B、C三份,各加入一定量的铁粉,充分反应后过滤、洗涤,分别得到滤渣和滤液.(1)若将A得到的滤渣加入稀盐酸中有气泡产生,则其滤液中的溶质是Fe(NO3)2;
(2)若将B得到的滤渣加入稀盐酸中没有气泡产生,则其滤渣中一定有Ag;
(3)若向C得到的滤液中滴加稀盐酸,有白色沉淀生成,则此滤液中含有的溶质是Fe(NO3)2、AgNO3和Cu(NO3)2.
分析 根据金属活动性顺序的应用及物质间的反应回答,铁铜银的活动性为铁>氢>铜>银,故铁能和AgNO3和Cu(NO3)2反应,溶液中有两种金属离子时,铁粉首先要置换金属活动性弱的金属--银,反应进行的程度由各物质的量的多少决定.
解答 解:(1)若将A得到的滤渣加入到稀盐酸中有气泡产生,说明滤渣中含有铁,铁有剩余,AgNO3和Cu(NO3)2两种溶质就完全反应,那么滤液中的溶质就只有Fe(NO3)2;
(2)若将B得到的滤渣加入到稀盐酸中没有气泡产生,说明铁没有剩余,有没有铜,不能确定,因为铁在溶液中会先置换活动性弱的银,故滤渣中一定很有银;
(3)若向C得到的滤液中滴加稀盐酸,有白色沉淀生成,说明滤液中含有AgNO3,那么铁就完全反应且铁的量少,只能置换一部分的银,硝酸铜还没有发生反应,故滤液中的溶质有Fe(NO3)2、AgNO3和Cu(NO3)2.
答案:(1)Fe(NO3)2;
(2)Ag;
(3)Fe(NO3)2、AgNO3和Cu(NO3)2.
点评 如果溶液是两种金属的盐溶液,另一种活泼金属置换溶液中的金属时,先置换活动性弱的金属.

练习册系列答案
相关题目
3.生活中常常可以用化学知识来解决一些问题,下列家庭小实验不合理的是 ( )
| A. | 用食醋除去暖水瓶中的薄层水垢 | |
| B. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 | |
| C. | 用食用碱(Na2CO3)溶液洗涤餐具上的油污 | |
| D. | 用米汤检验含碘盐中的碘酸钾(KIO3) |
4. 用“○”和“●”代表两种不同的原子,在一定条件下由这两种原子构成的分子发生以下的反应,反应前后的模拟模型如图所示,下列说法正确的是( )
用“○”和“●”代表两种不同的原子,在一定条件下由这两种原子构成的分子发生以下的反应,反应前后的模拟模型如图所示,下列说法正确的是( )
 用“○”和“●”代表两种不同的原子,在一定条件下由这两种原子构成的分子发生以下的反应,反应前后的模拟模型如图所示,下列说法正确的是( )
用“○”和“●”代表两种不同的原子,在一定条件下由这两种原子构成的分子发生以下的反应,反应前后的模拟模型如图所示,下列说法正确的是( )| A. | 该反应是化合反应 | |
| B. | 参加反应的“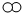 ”和“ ”和“ ”分子的个数比是 2:1 ”分子的个数比是 2:1 | |
| C. | 该反应生成物是混合物 | |
| D. | 该反应不遵循质量守恒定律 |
1.下列事实不能说明“分子间存在间隔”的是( )
| A. | 氧气被压缩后可装在钢瓶中 | |
| B. | 50mL水与50mL酒精混合体积小于100mL | |
| C. | 热胀冷缩 | |
| D. | 水电解生成氢气和氧气 |
1.比较Ag、Pd、Zn、Mn、Cu五种金属的活动性顺序:
(1)根据常见金属的活动性顺序表可知其中Ag、Zn、Cu金属的活动性由强至弱的顺序为Zn、Cu、Ag;(填元素符号)
(2)通过实验确定Pd、Mn的活动性:
步骤一:通过金属与稀盐酸作用初步判断Pd、Mn的活动性
步骤二:通过金属与盐溶液作用比较Ag、Pd、Cu的活动性
(3)若要确切的得出五种金属的活动性顺序,还应补充的一个实验是Mn片与ZnSO4溶液的反应(或Zn与MnCl2溶液的反应).
(1)根据常见金属的活动性顺序表可知其中Ag、Zn、Cu金属的活动性由强至弱的顺序为Zn、Cu、Ag;(填元素符号)
(2)通过实验确定Pd、Mn的活动性:
步骤一:通过金属与稀盐酸作用初步判断Pd、Mn的活动性
| 实验操作 | 实验现象 | 实验结论或化学方程式 |
| 将Mn片、Pd片 分别放入稀盐酸中 | Mn片表面有气泡产生,Pb片无明显现象 | 活动性:Mn>H>Pd |
| 实验操作 | 实验现象 | 化学方程式和实验结论 |
| 将Cu片浸入氯化钯(PdCl2)溶液中 | 铜丝表面覆盖一层银白色固体 | 化学方程式:Cu+PbCl2=Pb+CuCl2 |
| 将Ag片浸入PdCl2溶液中 | 无明显现象 | 实验结论:Ag的活动性比Pb弱 |
| 结论 | Pd、Cu、Ag金属活动性由强至弱:Cu、Pb、Ag | |
8.有甲、乙、丙三种金属,甲的盐溶液能用乙容器盛放,而不能用丙容器盛放,则三种金属的活动性顺序由弱到强的是( )
| A. | 甲、乙、丙 | B. | 丙、甲、乙 | C. | 乙、甲、丙 | D. | 乙、丙、甲 |
6.如图是镁和氯两种元素的有关信息,则下列说法错误的是( )

| A. | 氯元素的质子数为17 | |
| B. | 镁是金属元素、氯是非金属元素 | |
| C. | 镁和氯组成化合物的化学式为MgCl | |
| D. | 镁原子结构示意图中X=8,其电子的能量高于第一层 |