题目内容
我们常用原子利用率来衡量化学反应过程的原子经济性,其计算公式为:原子利用率=
×100%下面是联合工艺法制备新型自来水消毒剂ClO2的反应原理:
①电解氯化钠溶液NaCI+3H2O
NaC1O3+3H2↑
②氢气与氯气合成氯化氢
③生成二氧化氯 2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O
此方法的原子利用率最大为( )
| 目标生成物的质量 |
| 参加该反应所有反应物的总质量 |
①电解氯化钠溶液NaCI+3H2O
| ||
②氢气与氯气合成氯化氢
③生成二氧化氯 2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O
此方法的原子利用率最大为( )
分析:将反应的方程式整理得出总的反应方程式,根据方程式求出相对分子质量或相对分子质量和,根据题中信息公式可求出利用率
解答:解:②反应的方程式为H2+Cl2
2HCl,将方程式③+2×①+②×2再整理,可以得到总反应方程式:
Cl2+4H2O=2ClO2+4H2
总方程式可以看出,反应物的相对分子质量和是143生成的目标产物ClO2的相对分子质量是135,
×100%=
94.4%
故选D
| ||
Cl2+4H2O=2ClO2+4H2
总方程式可以看出,反应物的相对分子质量和是143生成的目标产物ClO2的相对分子质量是135,
| 135 |
| 143 |
94.4%
故选D
点评:本题考查根据化学方程式计算,根据信息确定出生成物和所有反应物的总的相对分子质量即可求出.

练习册系列答案
相关题目

 下面是联合工艺法制备新型自来水消毒剂ClO2的反应原理:
下面是联合工艺法制备新型自来水消毒剂ClO2的反应原理: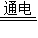 NaC1O3+3H2↑
NaC1O3+3H2↑