题目内容
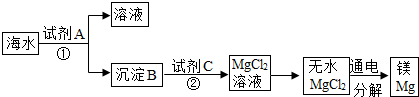
7.已知NaOH容易与空气中的CO2作用而变质.小军同学在实验室发现一瓶敞口放置的NaOH固体后,设计方案,对这瓶NaOH固体变质情况进行了如下实验探究: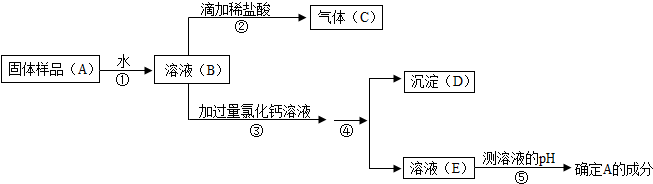
回答下列问题:
(1)上述实验操作①的名称是:溶解,其中玻璃棒的作用是搅拌,加速溶解.
(2)过滤所需的玻璃仪器有漏斗、烧杯、玻璃棒.
(3)根据上述实验,可以确定该固体已变质(选填“已”或“未”).
(4)步骤③中加过量氯化钙溶液的目的是完全除去碳酸钠.
分析 (1)根据每一步操作的目的判断操作的名称:①是将固体变成液体; 其中玻璃棒的作用是搅拌,加速溶解;
(2)根据过滤所需仪器分析解答;
(3)根据②中滴加稀盐酸可以判断有碳酸钠的存在,从而判断是否发生变质;
(4)NaOH固体变质的原因主要是与二氧化碳发生了反应产生碳酸钠,为探究固体中是否还含有NaOH,由于碳酸钠溶液也显碱性,故要先排除碳酸钠的干扰;
解答 解:(1)①是将固体加水变成溶液,故操作是:溶解;
其中玻璃棒的作用是故操作是搅拌,加速溶解;
(2)过滤所需的玻璃仪器有漏斗、烧杯、玻璃棒;
(3)②中滴加稀盐酸产生气体,是碳酸钠和盐酸反应产生的二氧化碳,因此可以判断有碳酸钠的存在,所以氢氧化钠固体已经发生变质;故答案为;已;
(4)为探究固体中是否还含有NaOH,由于碳酸钠溶液也显碱性,故要先排除碳酸钠的干扰;因此过量的CaCl2溶液可将碳酸钠全部反应掉,滴加足量的CaCl2溶液目的是:除尽溶液中的碳酸钠;
答案:
(1)溶解; 搅拌,加速溶解; (2)烧杯;玻璃棒; (3)已; (4)完全除去碳酸钠;
点评 本题考查了氢氧化钠的变质及变质程度的检验,要注意二者的不同,在进行验证变质程度时,要注意碳酸钠的碱性对氢氧化钠碱性的干扰.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
15.下列事实与对应解释不相符合的是( )
| A. | 氧化汞分解成汞和氧气--分子可以再分 | |
| B. | 甘蔗甜,苦瓜苦--不同分子性质不同 | |
| C. | 切洋葱时可闻到刺激性气味--分子在不停运动 | |
| D. | 结冰的水不能流动(0℃以下)--水分子不再运动 |
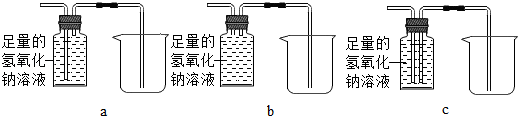
16. 某化学兴趣小组的同学对一些小食品的包装方式产生了兴趣.食品装在充满气体的小塑料袋里,这种充气的包装技术主要是为了能使食品较长时间地保质、保鲜.那么,其中充的是什么气体呢?
某化学兴趣小组的同学对一些小食品的包装方式产生了兴趣.食品装在充满气体的小塑料袋里,这种充气的包装技术主要是为了能使食品较长时间地保质、保鲜.那么,其中充的是什么气体呢?
【猜想与假设】小文说:该气体可能是CO2、O2、N2、空气.
小航说:不可能含有O2,因为氧气的化学性质比较活泼,会加速食品变质.
【查阅资料】(1)镁条可以在氮气中燃烧,生成物(Mg3N2)与水反应可以产生使湿润的红色石蕊试纸变蓝的物质(NH3).
(2)镁条在空气中燃烧主要生成氧化镁而不是氮化镁.
【进行实验】收集三瓶包装袋内的气体进行实验.请你填写下列表格.
【得出结论】这一批次食品包装袋中的气体是空气.
【反思】你认为食品充气包装中,对所充气体的要求是(写两点)
①无毒; ②价廉易得(合理即可).
 某化学兴趣小组的同学对一些小食品的包装方式产生了兴趣.食品装在充满气体的小塑料袋里,这种充气的包装技术主要是为了能使食品较长时间地保质、保鲜.那么,其中充的是什么气体呢?
某化学兴趣小组的同学对一些小食品的包装方式产生了兴趣.食品装在充满气体的小塑料袋里,这种充气的包装技术主要是为了能使食品较长时间地保质、保鲜.那么,其中充的是什么气体呢?【猜想与假设】小文说:该气体可能是CO2、O2、N2、空气.
小航说:不可能含有O2,因为氧气的化学性质比较活泼,会加速食品变质.
【查阅资料】(1)镁条可以在氮气中燃烧,生成物(Mg3N2)与水反应可以产生使湿润的红色石蕊试纸变蓝的物质(NH3).
(2)镁条在空气中燃烧主要生成氧化镁而不是氮化镁.
【进行实验】收集三瓶包装袋内的气体进行实验.请你填写下列表格.
| 猜想 | 验证方法 | 现象 |
| 空气 | 将燃着的木条伸入集气瓶中 | 木条正常燃烧 |
| CO2 | 无明显现象 | |
| N2 | 无明显现象 |
【反思】你认为食品充气包装中,对所充气体的要求是(写两点)
①无毒; ②价廉易得(合理即可).
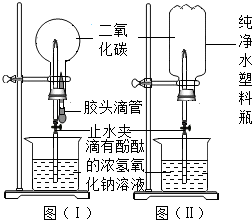
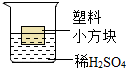 向如图所示的烧杯中先滴入两滴酚酞试液,然后在不断搅拌的情况下逐滴加入Ba(OH)2溶液,直至过量.在这个过程中,请回答下列问题:
向如图所示的烧杯中先滴入两滴酚酞试液,然后在不断搅拌的情况下逐滴加入Ba(OH)2溶液,直至过量.在这个过程中,请回答下列问题: