题目内容
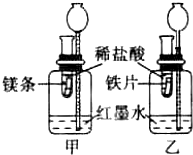 小冰和小城在老师的帮助下组装了如图所示的实验装置,在室温条件下,他们进行了下面实验:先在试管内放相同的稀盐酸,同时向两支试管中加入形状质量相同的镁片和铁片.
小冰和小城在老师的帮助下组装了如图所示的实验装置,在室温条件下,他们进行了下面实验:先在试管内放相同的稀盐酸,同时向两支试管中加入形状质量相同的镁片和铁片. (1)实验后比较,甲、乙两装置中不同的实验现象是
(2)请你解释甲装置产生该实验现象的原因
考点:金属的化学性质
专题:金属与金属材料
分析:在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,且金属活动性越强,与酸反应的速率越快,单位时间内放出的热量多,据此结合题意进行分析解答即可.
解答:解:在试管内放相同的稀盐酸,同时向两支试管中加入形状质量相同的镁片和铁片,从装置图看出,甲乙装置都是密闭的系统,因为镁的金属活动性比铁强,与酸反应快,单位时间内产生的氢气多,放出的热量多,密闭装置内压强大,所以会观察到甲中长颈漏斗里的液面上升得更快.
故答案为:(1)甲中长颈漏斗里的液面上升得更快;(2)镁的金属活动性比铁强,与酸反应快,单位时间内产生的氢气多,放出的热量多.
故答案为:(1)甲中长颈漏斗里的液面上升得更快;(2)镁的金属活动性比铁强,与酸反应快,单位时间内产生的氢气多,放出的热量多.
点评:本题难度不大,掌握金属的化学性质并能灵活运用是正确解答本题的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列实验方案不能达到实验目的是( )
| A、区别CO2和CO:分别通入紫色石蕊溶液 |
| B、用水区分碳酸钙粉末和碳酸钠粉末 |
| C、分离BaCl2和NaCl的混合溶液:加适量Na2CO3溶液,充分反应后过滤 |
| D、用稀盐酸清除铁制品表面的铁锈 |

 金属材料在生活中使用广泛.
金属材料在生活中使用广泛.