题目内容
17.如图是实验室制取二氧化碳气体可能用到的实验装置.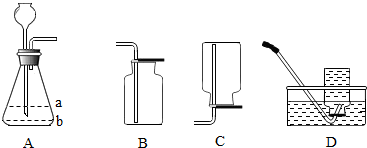
(1)制取二氧化碳气体时,锥形瓶内液体应加至a(选填“a”或“b”)处.
(2)收集二氧化碳气体应选用的装置是B.
分析 (1)根据使用长颈漏斗时要防止生成的气体从长颈漏斗中逸出,进行分析解答.
(2)根据二氧化碳的密度比空气的大,能溶于水,进行分析解答.
解答 解:(1)制取二氧化碳气体时,为防止生成的二氧化碳气体从长颈漏斗中逸出,长颈漏斗应伸入液面以下,锥形瓶内液体应加至a.
(2)二氧化碳的密度比空气的大,能溶于水,所以应该选择B装置来收集二氧化碳.
故答案为:(1)a;(2)B.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取二氧化碳的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
7.某同学要完成纯净的氨气与灼热的氧化铜的反应(2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2),图中(夹持、固定装置均略去)仪器连接顺序最合适的是( )
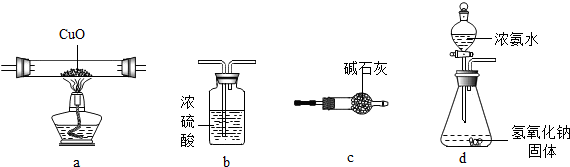

| A. | dabc | B. | dcab | C. | dbac | D. | dacb |
5.有关氧气化学性质的描述中,不正确的是( )
| A. | 氧气的化学性质活泼 | B. | 氧气能供给呼吸 | ||
| C. | 氧气能支持燃烧 | D. | 氧气能做燃料 |
2.科学兴趣小组的同学为了测定某铜铁合金的组成,取20克样品于烧杯中,向其中分4次加入相同溶质质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量及剩余固体的质量记录如下表:
请分析回答下列问题:
(1)上述表格中m的值为12.0.
(2)此样品中铁的质量分数为40%.
(3)所用稀硫酸中硫酸的质量分数是多少?
| 实验序号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀硫酸的质量(克) | 20 | 20 | 20 | 20 |
| 充分反应后剩余固体的质量(克) | 17.2 | 14.4 | 12.0 | m |
(1)上述表格中m的值为12.0.
(2)此样品中铁的质量分数为40%.
(3)所用稀硫酸中硫酸的质量分数是多少?
9.比较归纳是科学学习中的常用方法.若以下的物质转化都由一步反应完成:①Mg→MgCl2 ②Mg(OH)2→MgCl2 ③MgCO3→MgCl2.则( )
| A. | 三种转化发生的都是复分解反应 | B. | 三种转化都必须加入盐酸才能进行 | ||
| C. | 只有②发生了中和反应 | D. | 三种转化的生成物中都有水 |
13.下列化学实验基本操作正确的是( )
| A. | 把橡皮塞慢慢转动着塞进容器口 | |
| B. | 向燃着的酒精灯里添加酒精 | |
| C. | 滴瓶上的滴管用过后,先用水洗净再放回滴瓶 | |
| D. | 组装仪器时,一般遵循的原则是:从左到右,先上后下 |