题目内容
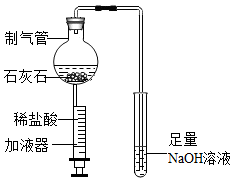
8.请根据下列装置,回答问题:(1)写出标号①的仪器名称:①长颈漏斗.
(2)用高锰酸钾制取O2时,用A、D进行实验,写出该反应化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
发现水槽中的水变红的原因为试管口没有塞棉花.
气体收集完毕时,应先从水中取出导管(填“从水中去除导气管”或“熄灭酒精灯”)
(3)某同学在实验室制二氧化碳气体时,写出该反应化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.将气体的发生装置由B改进为F,这样做的好处是可以随时控制反应的发生和停止.
(4)实验室用固体无水醋酸钠和碱石灰混合物加热的方法制取甲烷.该实验可选用的发生装置是A,收集装置是可选择D或E.
(5)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液.向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有Ag(填化学式),滤液中一定含有的溶质是Fe(NO3)2(填化学式)

分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室用固体无水醋酸钠和碱石灰混合物加热的方法制取甲烷,因此需要加热;甲烷的密度比空气小,极难溶于水,因此能用向下排空气法和排水法收集;向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液.向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有银,可能含有铜,一定没有铁粉;滤液中一定含有的溶质是硝酸亚铁.
解答 解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;发现水槽中的水变红的原因为试管口没有塞棉花,气体收集完毕时,应先从水中取出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂,故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;试管口没有塞棉花;从水中取出导管;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;F装置的优点是:可以随时控制反应的发生和停止;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;可以随时控制反应的发生和停止;
(4)实验室用固体无水醋酸钠和碱石灰混合物加热的方法制取甲烷,因此需要加热;甲烷的密度比空气小,极难溶于水,因此能用向下排空气法和排水法收集;故答案为:A;D或E;
(5)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液.向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有银,可能含有铜,一定没有铁粉;滤液中一定含有的溶质是硝酸亚铁;故答案为:Ag;Fe(NO3)2;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、注意事项和混合物的分离等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

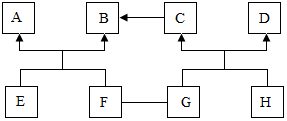

 化学兴趣小组设计了如图所示的微型实验.
化学兴趣小组设计了如图所示的微型实验.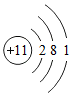 ,它的电子数为11.
,它的电子数为11.