题目内容
11.根据如图部分金属的活动性顺序回答:
(1)如图金属中活动性最强的是Mg;
(2)按年代最早被广泛使用的金属是Cu;
(3)已知:①X+H2SO4═XS04+H2↑;②Y+2ZNO3═Y(NO3)2+2Z;③Y与稀硫酸不反应:则符合要求的X、Y、Z分别是B(填字母序号).
A.Cu、Hg、Ag B.Fe、Cu、Ag C.Mg、Zn、Fe.
分析 根据金属活动性顺序的运用分析回答,金属的位置越靠前,金属的活动性就越强,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能把位于其后的金属从其盐溶液中置换出来.
解答 解:(1)由图示可知,金属中活动性最强的是Mg;
(2)按年代最早被广泛使用的金属是Cu;
(3)由①X+H2SO4═XS04+H2↑,说明了X位于氢的前边,在化合物中X的化合价为+2;由②Y+2ZNO3═Y(NO3)2+2Z,说明了Y位于Z的前边,在化合物中Y、Z的化合价分别是+2、+1;③Y与稀硫酸不反应,说明了Y位于氢的后面,则金属的活动性强弱是:X>Y>Z,符合要求的分别是:Fe、Cu、Ag.所以B正确.
故答为:(1)Mg;(2)Cu;(3)B.
点评 本题考查了金属活动性顺序的运用,难度不大,熟练掌握活动性的内容及在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能把位于其后的金属从其盐溶液中置换出来是解题的关键.

练习册系列答案
相关题目
2.下列四组溶液不另加试剂就能鉴别的是( )
| A. | BaCl2、NaCl、H2SO4、K2CO3 | B. | Na2SO4、NaCl、Ba(OH)2、KNO3 | ||
| C. | NaOH、K2SO4、NaCl、Ba(NO3)2 | D. | Ba(NO3)2、NaCl、Ca(OH)2、Na2CO3 |
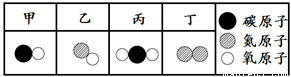
19.下列对宏观现象的微观解释错误的是( )
| A. | CO与CO2化学性质不同,是因为它们的分子构成不同 | |
| B. | NaOH溶液与KOH溶液都能使酚酞溶液变成红色,是因为它们的溶液中都含有OH- | |
| C. | 金刚石和石墨物理性质存在差异,是因为构成它们的碳原子不同 | |
| D. | 温度计受热时,水银柱上升,是因为受热时汞原子间间隔变大 |
20.某校兴趣小组对氢氧化钠溶液与稀盐酸混合后的有关问题,进行了如下探究,请你一起参与此次探究活动.
(1)探究一:氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
[方案设计]小亮、小丽两位同学设计了如下方案进行探究:
[方案评价]小林同学认为以上设计的两个方案中只有一个正确,你认为小丽同学的方案正确,另外一个方案错误的原因是若加入的稀盐酸过量,溶液呈酸性,酚酞溶液也不会变色.
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
[作出猜想]小亮猜想:溶质有NaCl、HCl、NaOH;小丽猜想:溶质只有NaCl;
小林猜想:溶质有NaCl、NaOH;你的猜想:溶质有NaCl、HCl(填化学式).
小丽认为小亮的猜想是错误的,她的理由是氢氧化钠和稀盐酸在同一溶液中不能共存(或氢氧化钠和稀盐酸能发生化学反应).
[实验设计及验证]请你将下列实验报告填写完整:
(1)探究一:氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
[方案设计]小亮、小丽两位同学设计了如下方案进行探究:
| 方案 设计者 | 方案步骤 | 方案预估现象 | 方案 预估结论 |
| 小亮 | 取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡 | 酚酞试液 不变色 | 恰好完全中和 |
| 小丽 | 用一根洁净的玻璃棒蘸取反应后的溶液沾在pH试纸上,把试纸呈现的颜色与标准比色卡对照 | pH=7 | 恰好完全中和 |
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
[作出猜想]小亮猜想:溶质有NaCl、HCl、NaOH;小丽猜想:溶质只有NaCl;
小林猜想:溶质有NaCl、NaOH;你的猜想:溶质有NaCl、HCl(填化学式).
小丽认为小亮的猜想是错误的,她的理由是氢氧化钠和稀盐酸在同一溶液中不能共存(或氢氧化钠和稀盐酸能发生化学反应).
[实验设计及验证]请你将下列实验报告填写完整:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入碳酸钠溶液 | 气体生成 | 你的猜想正确 |
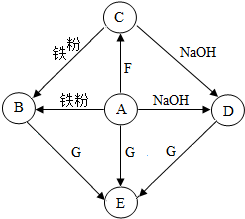 A-G是初中化学常见物质,其中,A的浓溶液能挥发处刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀,如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
A-G是初中化学常见物质,其中,A的浓溶液能挥发处刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀,如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.