题目内容
有一包含杂质的碳酸钠固体粉末,为测定混合物中碳酸钠的含量,取10g样品于烧杯中,向其中加入足量的氯化钡溶液(杂质不反应,也不溶于水),反应结束后将烧杯内液体过滤烘干得到14.55g滤渣,求样品中碳酸钠的含量是( )
| A、53% | B、10.6% |
| C、46% | D、80% |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:该题中所发生的反应为碳酸钠和氯化钡的反应,反应生成了碳酸钡沉淀,可以利用差量法来解答该题.
解答:解:设样品中碳酸钠质量为x
Na2CO3+BaCl2═BaCO3↓+2NaCl 固体质量差
106 197 197-106=91
x 14.55g-10g=4.55g
=
x=5.3g
样品中碳酸钠的含量是=
×100%=53%
故选择A.
Na2CO3+BaCl2═BaCO3↓+2NaCl 固体质量差
106 197 197-106=91
x 14.55g-10g=4.55g
| 91 |
| 4.55g |
| 106 |
| x |
x=5.3g
样品中碳酸钠的含量是=
| 5.3g |
| 10g |
故选择A.
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后根据所给的问题情景细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
相关题目
2014年南京青奥会火炬使用的燃料为A物质,纯净物A在B物质中充分燃烧,发生反应:A+5B
3C+4D(部分微观示意图如下所示)
下列说法不正确的是( )
| ||
| 物质 | A | B | C | D | 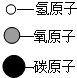 |
| 分子示意图 | ? |  |  |  |
| A、A物质中含有碳、氢、氧三种元素 |
| B、A物质中含有碳、氢原子个数比为3:8 |
| C、A物质具有可燃性,B物质具有氧化性 |
| D、该反应既不是化合反应也不是分解反应 |
关于分子和原子两种微粒的叙述正确的是( )
| A、物质只能由分子构成 |
| B、分子可分为原子,原子不可再分 |
| C、相同原子可能构成不同分子 |
| D、化学变化中分子数目一定发生变化 |
下列物质中,含有氧分子的是( )
| A、O2 |
| B、H2O2 |
| C、SO2 |
| D、NO2 |
 鸡蛋壳主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半.试计算(计算结果保留1位小数):(盐酸是HCl溶于水形成的溶液,反应中水不参加反应)
鸡蛋壳主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半.试计算(计算结果保留1位小数):(盐酸是HCl溶于水形成的溶液,反应中水不参加反应) 可知,氮原子最外层电子数目为
可知,氮原子最外层电子数目为