题目内容
有一含纯碱的食盐样品,为了测定其中碳酸钠的含量,某同学称取30 g样品放入烧杯中,向烧杯中加入100 g足量的稀盐酸,充分反应后烧杯中剩余物的总质量为123.4 g(假设产生的气体全部逸出)
g(假设产生的气体全部逸出)
(1 )反应生成的气体的质量为__g;
)反应生成的气体的质量为__g;
(2)样品中碳酸钠的质量分数是多少?
6.6
解:(1)根据质量守恒定律,可得出生成的二氧化碳的质量为:30 g+100 g-123.4 g=6.6 g (2)设30 g样品中碳酸钠的质量为x
Na2CO3+2HCl===2NaCl+H2O+CO2↑
106 44
x 6.6 g
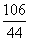 =
=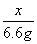
x=15.9 g
样品中碳酸钠的质量分数是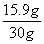 ×100%=53%
×100%=53%

练习册系列答案
相关题目

 、过滤等操作。请从图三中选出这两种操作均不会用到的仪器是__ __(填序号)。
、过滤等操作。请从图三中选出这两种操作均不会用到的仪器是__ __(填序号)。

 )
)