题目内容
15. 如图是A、B、C三种物质的溶解度曲线,据图回答:
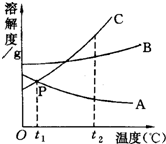
如图是A、B、C三种物质的溶解度曲线,据图回答:(1)P点表示t1℃时A、C物质的溶解度相等.
(2)溶解度随温度升高而减少的物质是A.
(3)t2℃时,三种物质的溶解度由大到小的顺序是C>B>A.
(4)t1℃时A的溶解度大于t2℃时A的溶解度(填“大于”、“小于”或“等于”).
(5)若C的溶液中含有少量的B,从溶液中分离出C的方法是冷却热饱和溶液.
分析 (1)根据溶解度曲线的交点表示该温度下两物质的溶解度相等进行解答;
(2)判断某物质的溶解度受温度影响变化的趋势,据此分析解答;
(3)根据固体溶解度曲线的意义及固体的溶解度和温度之间的关系解答;
(4)利用物质的溶解度曲线,比较物质在不同温度下的溶解度的大小;
(5)物质的溶解度受温度影响的情况及分离混合物物的方法.
解答  解:(1)P点的含义是t1℃时A、C两物质的溶解度相等.
解:(1)P点的含义是t1℃时A、C两物质的溶解度相等.
故填:A、C;
(2)如图所示,物质A的溶解度随温度升高而减少.
故填:A.
(3)有三物质的溶解度曲线可知:三物质在t2℃时的溶解度大小关系是:C>B>A,
故填:C>B>A.
(4)A物质的溶解度随温度升高而减小,由于t2℃>t1℃,所以t1℃时A物质的溶解度大于t2℃时A的溶解度.
故填:大于;
(5)由C、B物质的溶解度曲线可知:C物质的溶解度受温度的影响较大,B物质的溶解度受温度的影响不大.所以,从C、B的混合物中分离A物质,一般采用冷却热饱和溶液的方法.
故填:冷却热饱和溶液.
点评 本题难度不大,主要考查了固体溶解度曲线的意义及根据固体溶解度曲线解决相应的问题,从而培养学生的理解能力和解决问题的能力.

练习册系列答案
相关题目
6.下列变化中,属于化学变化的是( )
| A. | 酒精挥发 | B. | 潮湿的衣服变干 | C. | 水结冰 | D. | 铁器生锈 |
20.下列分子的叙述中,错误的是( )
| A. | 分子是构成物质的一种微粒 | |
| B. | 分子是不断运动的 | |
| C. | 物质发生变化时,分子也一定发生变化 | |
| D. | 固态物质分子间也存在间隔 |
4. 已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O
已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O
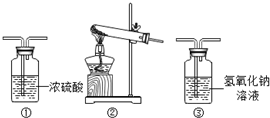
某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.
(1)实验用到的主要装置为如图所示:装置连接顺序为②→①→③.(填写编号)
(2)操作步骤及数据处理:
第一步 检查气密性;
第二步 装入药品,称取装置①和③的质量;
第三步 试验后再次称取装置①和③的质量,记录数据如表:
根据以上数据可得产生的水和二氧化碳的质量之比为21:44.(要求写出最简整数比)
(3)结果分析;从下列选项中选出产生该实验结果可能的原因有哪些?AC
A.二氧化碳没有被完全吸收 B.水没有被完全吸收
C.碱式碳酸铜药品中含有水分 D.碱式碳酸铜没有完全分解.
 已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O
已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.
(1)实验用到的主要装置为如图所示:装置连接顺序为②→①→③.(填写编号)
(2)操作步骤及数据处理:
第一步 检查气密性;
第二步 装入药品,称取装置①和③的质量;
第三步 试验后再次称取装置①和③的质量,记录数据如表:
| 装置 质量 时间 | 装置① | 装置③ |
| 实验前 | 220.0克 | 195.0克 |
| 实验后 | 222.1克 | 199.4克 |
(3)结果分析;从下列选项中选出产生该实验结果可能的原因有哪些?AC
A.二氧化碳没有被完全吸收 B.水没有被完全吸收
C.碱式碳酸铜药品中含有水分 D.碱式碳酸铜没有完全分解.
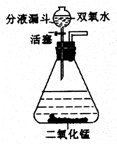 过氧化氢俗称双氧水,常温下是一种无色液体,它与二氧化锰混合后能迅速释放出氧气.此反应中二氧化锰作催化剂.在实验室中可用如图所示装置制取氧气.
过氧化氢俗称双氧水,常温下是一种无色液体,它与二氧化锰混合后能迅速释放出氧气.此反应中二氧化锰作催化剂.在实验室中可用如图所示装置制取氧气.