题目内容
8.如图为用镀锌铁片制成的日常用品.镀锌铁是指通过镀锌工艺在铁皮上进行镀锌而制成的一种产品,热镀锌产品广泛用于建筑、家电、车船、容器制造业、机电业等,几乎涉及衣食住行各个领域.为测定铁片镀锌层的厚度实验过程如下.
【实验步骤】
(1)剪取一片镀锌铁片,量得长度=2.0cm,宽度=l.9cm.
(2)用电子天平称量质量0.857g.
(3)实验中需要溶质质量分数为10%的稀盐酸200mL(密度=1.05g/mL),需要量取溶质质量分数为37%的浓盐酸(密度=1.18g/mL)48.1(保留至小数点后1位)mL,然后稀释.
(4)将镀锌铁片放入溶质质量分数为10%盐酸中.当观察到气泡产生的速率突然减慢,可以判断镀锌层恰好反应.
(5)将溶液中的铁片取出清洗、擦干、烘干后用电子天平称量质量0.837g.
【计算结果】
(1)铁片镀锌层的质量有0.02g.
(2)已知锌的密度7.1g/cm3,计算出铁片镀锌层厚度0.37mm.
【实验反思】
实际计算结果偏大,同学们分析,这是因为很难通过观察现象判断镀锌层恰好反应,造成镀锌铁片浸泡在盐酸中时间偏长(填“偏长”或“偏短”).
【实验改进】
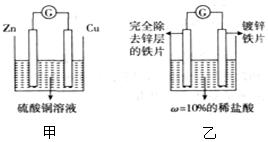
资料卡片:如图甲所示,两种金属活动性不同的金属放入酸、碱、盐溶液中,会有电子的流动,从而产生电流.
将上述实验改进成如图乙的装置,当观察到电流计指针指向0,此时锌层恰好反应.
分析 【实验步骤】
溶液稀释前后,溶质质量不变;
锌比铁活泼,因此锌和稀盐酸反应的速率比铁快;
【计算结果】
根据提供的数据可以进行相关方面的计算;
【实验反思】
如果铁也和稀盐酸反应,会导致计算的锌的质量偏大,从而导致实际计算结果偏大;
【实验改进】
将上述实验改进成如图乙的装置,当观察到电流为零时,锌层恰好反应.
解答 解:【实验步骤】
(3)需要量取溶质质量分数为37%的浓盐酸体积为:1.05g/mL×200mL×10%÷1.18g/mL÷37%=48.1mL,
(4)将镀锌铁片放入溶质质量分数为10%盐酸中.当观察到气泡产生的速率突然减慢,可以判断镀锌层恰好反应.
故填:气泡产生的速率突然减慢.
【计算结果】
(1)铁片镀锌层的质量有:0.857g-0.837g=0.02g.
故填:0.02.
(2)铁片镀锌层厚度为:0.02g÷(2.0cm×1.9cm×7.1g/cm3)÷2=0.37mm.
故填:0.37.
【实验反思】
实际计算结果偏大,同学们分析,这是因为很难通过观察现象判断镀锌层恰好反应,造成镀锌铁片浸泡在盐酸中时间偏长,导致部分铁参加反应,
故填:偏长.
【实验改进】
将上述实验改进成如图乙的装置,当观察到电流计指针指向0,即电流为零时,锌层恰好反应.
故填:电流计指针指向0.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
19.下列说法中正确的是( )
| A. | Fe、Fe2+、Fe3+三种粒子的性质相同 | |
| B. | 水是由氢气、氧气组成的氧化物 | |
| C. | 空气、氯化钠、水银是按混合物、化合物、单质顺序排列的 | |
| D. | 水通电分解和水的蒸发都是化学变化 |
16.某物质R是人类生命活动中不可缺少的物质.已知R的相对分子质量为150,其中含碳元素40%,含氢元素6.7%,其余为氧元素.则R的化学式为( )
| A. | C5H10O2 | B. | C6H6O | C. | C5H10O5 | D. | C6H12O6 |
13.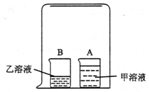 老师在课堂上演示了一个有趣的实验:在一只洁净的小烧杯A中装入30ml蒸馏水,再滴入2-3滴石蕊试液(甲溶液);在小烧杯B中装入30mL浓盐酸(乙溶液);用一个玻璃水槽把A、B两个烧杯罩在一起,一会儿就看到A烧杯中的溶液变成了红色.
老师在课堂上演示了一个有趣的实验:在一只洁净的小烧杯A中装入30ml蒸馏水,再滴入2-3滴石蕊试液(甲溶液);在小烧杯B中装入30mL浓盐酸(乙溶液);用一个玻璃水槽把A、B两个烧杯罩在一起,一会儿就看到A烧杯中的溶液变成了红色.
同学们对上述现象看法不一,有以下两种猜测:
第一种:A烧杯中的蒸馏水使石蕊试液变成了红色.
第二种:B烧杯中的浓盐酸挥发出一种气体,溶解到A烧杯的溶液中,使溶液变成红色.
(1)你认为哪种猜测是正确的?如果你不同意以上两种猜测,请给出你的猜测.第二种.
(2)请你设计实验方案,证明(1)中你的猜测.提供的实验用品:烧杯、试管、胶头滴管、滤纸;蒸馏水、石蕊试液、浓盐酸、氯化氢气体等.
 老师在课堂上演示了一个有趣的实验:在一只洁净的小烧杯A中装入30ml蒸馏水,再滴入2-3滴石蕊试液(甲溶液);在小烧杯B中装入30mL浓盐酸(乙溶液);用一个玻璃水槽把A、B两个烧杯罩在一起,一会儿就看到A烧杯中的溶液变成了红色.
老师在课堂上演示了一个有趣的实验:在一只洁净的小烧杯A中装入30ml蒸馏水,再滴入2-3滴石蕊试液(甲溶液);在小烧杯B中装入30mL浓盐酸(乙溶液);用一个玻璃水槽把A、B两个烧杯罩在一起,一会儿就看到A烧杯中的溶液变成了红色.同学们对上述现象看法不一,有以下两种猜测:
第一种:A烧杯中的蒸馏水使石蕊试液变成了红色.
第二种:B烧杯中的浓盐酸挥发出一种气体,溶解到A烧杯的溶液中,使溶液变成红色.
(1)你认为哪种猜测是正确的?如果你不同意以上两种猜测,请给出你的猜测.第二种.
(2)请你设计实验方案,证明(1)中你的猜测.提供的实验用品:烧杯、试管、胶头滴管、滤纸;蒸馏水、石蕊试液、浓盐酸、氯化氢气体等.
| 实验(简述实验内容和方法) | 观察到的实验现象 |
| 1、用洁净的小烧杯取20mL水,滴入2-3滴紫色石蕊试液,观察现象; 2、取一张滤纸,滴入紫色石蕊试液,待晾干后,放在装上有浓盐酸的试剂瓶上方; 3、将少量氯化氢通入含有石蕊试液的蒸馏水中 | 不变色,水不能使石蕊试液变色; 不变色,氯化氢不能使石蕊试液变色; 变色,氯化氢溶解在水中形成的盐酸能使石蕊试液变色. |
20.下列有关空气的说法正确的是( )
| A. | 纯净的空气是混合物 | |
| B. | 空气中二氧化碳含量的增加,不会影响空气的质量 | |
| C. | 空气中水蒸气的体积分数为78% | |
| D. | 空气中的二氧化硫含量过高时,会造成温室效应 |
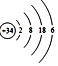 .硒单质是红色或灰色粉末,有灰色金属光泽,导电性随光照强度急剧变化,可制半导体和光敏材料.硒在空气中燃烧发出蓝色火焰,生成二氧化硒.工业上可以利用反应Na2SeSO3→Na2SO3+Se来制备硒单质.
.硒单质是红色或灰色粉末,有灰色金属光泽,导电性随光照强度急剧变化,可制半导体和光敏材料.硒在空气中燃烧发出蓝色火焰,生成二氧化硒.工业上可以利用反应Na2SeSO3→Na2SO3+Se来制备硒单质.