题目内容
13.将165克的稀盐酸加入盛有53g含有杂质的石灰石(杂质不与盐酸反应,也不溶于水)的烧杯中,恰好完全反应后烧杯中的总质量为196g.试计算:(1)反应生成二氧化碳的质量为22g.
(2)反应后所得溶液的溶质质量分数为多少?
分析 (1)根据质量守恒定律,反应前后减少的质量为二氧化碳的质量;
(2)由二氧化碳的质量根据碳酸钙与稀盐酸反应的化学方程式可以计算出发生反应的碳酸钙的质量和生成氯化钙的质量,结合烧杯中剩余物的质量可以计算出所得溶液中溶质的质量分数.
解答 解:(1)依据质量守恒定律可知,生成的CO2的质量为165g+53g-196g=22g
(2)设石灰石中碳酸钙的质量为x,生成氯化钙的质量为y.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
x y 22g
$\frac{100}{x}=\frac{111}{y}=\frac{44}{22g}$
x=50g,y=55.5g
生成物溶液中溶质的质量分数为:$\frac{55.5g}{196g-(53g-50g)}$×100%≈28.8%
答案:
(1)22.
(2)生成物溶液中溶质的质量分数为28.8%.
点评 根据化学方程式进行计算时,只能使用纯净物的质量进行计算,而不能把混合物的质量直接代入化学方程式进行计算,有关反应前后质量减少的计算是初中化学计算的一个常见内容,一般的规律是依据质量的变化求出某一生成的质量.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
4.实验时科学探究的重要方法,如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题.
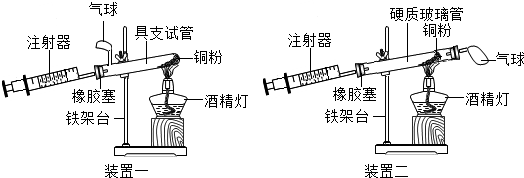
(1)根据下表提供的实验数据,完成下表.
(2)装置一和装置二中气球的位置不同,装置二(填“装置一”和“装置二”)更合理,理由是能让空气更易流通,全部通过铜粉,使氧气与铜粉充分反应.
(3)若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两条)铜粉的量不足;未待装置完全冷却至室温就读数.
(4)查阅资料得知,金属镁不仅能与空气中的氧气反应,还能与氮气反应,能否用镁粉代替铜粉来测定空气中氧气的含量不能(填“能”或“不能”),这会使测量的结果偏大(填“偏大”“偏小”或“不变”)
(5)实验反思:为测定空气中氧气含量而运用化学方法除去氧气时,应选择怎样的药品?应选择只能与氧气反应且不生成其他气体的药品.

(1)根据下表提供的实验数据,完成下表.
| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 25mL | 15mL | 9mL | 15% |
(3)若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两条)铜粉的量不足;未待装置完全冷却至室温就读数.
(4)查阅资料得知,金属镁不仅能与空气中的氧气反应,还能与氮气反应,能否用镁粉代替铜粉来测定空气中氧气的含量不能(填“能”或“不能”),这会使测量的结果偏大(填“偏大”“偏小”或“不变”)
(5)实验反思:为测定空气中氧气含量而运用化学方法除去氧气时,应选择怎样的药品?应选择只能与氧气反应且不生成其他气体的药品.