题目内容
1.我国铁矿石资源比较丰富,2000年,钢铁年总产量就已达到1.27亿吨,成为世界钢铁大国.某钢铁厂日产含4%杂质的生铁100t,则需要含Fe2O380%的赤铁矿多少吨?分析 由生铁的质量和含杂质的质量分数和赤铁矿中氧化铁的质量分数,根据一氧化碳与氧化铁反应的化学方程式可以计算出需要赤铁矿的质量.
解答 解:设需要赤铁矿的质量为x,
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
x×80% 100t×(1-4%)
$\frac{160}{112}=\frac{x×80%}{100t(1-4%)}$ 解得:x≈171.43t
答:需要含Fe2O380%的赤铁矿171.43t.
点评 本题主要考查有关含杂质物质的化学方程式计算,难度较大,注意带入方程的量必须是纯量.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
16.在稀盐酸中加入下列物质,溶液的pH几乎不变的是( )
| A. | 生石灰(CaO) | B. | CaCO3固体 | C. | KOH溶液 | D. | AgNO3溶液 |
17.下列图示实验操作中,正确的是( )
| A. | 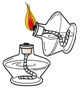 | B. | 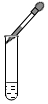 | C. |  | D. |  |
1.下列对宏观事实的微观解释正确的是( )
| 事 实 | 解 释 | |
| A | 硝酸钾溶于水消失了 | 分子不能运动 |
| B | 稀硫酸和稀盐酸都能使紫色石蕊溶液变红 | 它们在水溶液中解离出的阳离子都是H+ |
| C | 湿衣服在阳光下晾晒变干 | 水分子受热变成了氧气分子和氢气分子 |
| D | 装有红磷的密闭氧气瓶,点燃其中的红磷后,质量不变 | 反应前后瓶中分子总数不变 |
| A. | A | B. | B | C. | C | D. | D |
6.草莓,香蕉等水果具有芳香气味,是因为其中含有乙酸乙酯(化学式为C4H8O2),等物质,下列关于乙酸的说法正确的是( )
| A. | 乙酸乙酯属于氧化物 | |
| B. | 1个乙酸乙酯分子中含有4个水分子 | |
| C. | 乙酸乙酯中碳、氢、氧的质量比为4:8:2 | |
| D. | 乙酸乙酯燃烧有二氧化碳和水生成 |
11.把足量的铁粉,分别加入到下列各组物质的溶液中,充分反应后过滤,滤液中只有一种溶质的是( )
| A. | Na2SO4、CuSO4 | B. | HCl、CuCl2 | C. | HCl、H2SO4 | D. | CuCl2、CuSO4 |
