题目内容
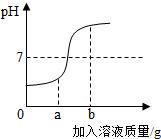 在用稀盐酸和氢氧化钠溶液进行反应实验时,过程中溶液的酸碱度变化如图所示.
在用稀盐酸和氢氧化钠溶液进行反应实验时,过程中溶液的酸碱度变化如图所示.(1)该实验操作是将
(2)当加入溶液的质量为ag时,所得溶液中的溶质为(写化学式)
考点:中和反应及其应用,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:(1)根据坐标变化的趋势结合盐酸的pH小于7,氢氧化钠溶液的pH大于7分析;
(2)当加入溶液的质量为ag时,溶液呈现酸性,溶液中既有生成的氯化钠,又有未反应的盐酸.
(2)当加入溶液的质量为ag时,溶液呈现酸性,溶液中既有生成的氯化钠,又有未反应的盐酸.
解答:解:
(1)坐标的pH变化是由小于7到大于7的过渡,因此进行的操作是将氢氧化钠溶液滴加到稀盐酸中,故答案为:氢氧化钠溶液;
(2)当加入溶液的质量为ag时,溶液呈现酸性,所得溶液中的溶质为氯化氢和氯化钠,
答案:
(1)氢氧化溶液
(2)NaCl HCl
(1)坐标的pH变化是由小于7到大于7的过渡,因此进行的操作是将氢氧化钠溶液滴加到稀盐酸中,故答案为:氢氧化钠溶液;
(2)当加入溶液的质量为ag时,溶液呈现酸性,所得溶液中的溶质为氯化氢和氯化钠,
答案:
(1)氢氧化溶液
(2)NaCl HCl
点评:本题考查了酸碱混合的定性判断、化学方程式的书写,题目难度中等,解答本题的关键是根据坐标的pH变化结合溶液的酸碱性与溶液pH的关系进行分析,并对反应过程中的溶液的酸碱性正确判断.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
意大利科学家最近获得了极具理论研究价值的N4分子.有关N4说法正确的是( )
| A、1个N4分子由2个N2分子构成 |
| B、N4是一种混合物 |
| C、N4和N2互为同素异形体 |
| D、N4的式量为56g |