题目内容
1.称取氯化钠和氯化钙的固体混合物14g,放入烧杯中,加入96g碳酸钠溶液恰好完全反应.待反应完全后过滤,称得滤液的总质量为100g.(1)根据质量守恒定律,可知生成沉淀的质量为10g.
(2)固体混合物中氯化钙的质量是多少?
(3)所得滤液中溶质的质量分数是多少?
分析 (1))由题意可知,滤液的总质量与生成沉淀的质量之和应等于反应前所有混合物的总质量.
(2)欲知固体混合物中CaCl2的质量,需分析题意,得出生成沉淀的质量,再根据化学方程式得出各物质之间的质量比,列出比例式,就可计算出固体混合物中氯化钙的质量;
(3)根据上述方程式可以求出生成NaCl的质量,滤液中的溶质还包括混合物中NaCl的质量,据此可以计算出滤液中溶质的质量,然后根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%计算即可.
解答 解:(1))由题意可知,滤液的总质量与生成沉淀的质量之和应等于反应前所有混合物的总质量.所以生成沉淀的质量=14g+96g-100g=10g;
(2)设固体混合物中氯化钙的质量为x,生成NaCl的质量为y.
CaCl2+Na2CO3=2NaCl+CaCO3↓
111 117 100
x y 10g
$\frac{111}{x}=\frac{117}{y}=\frac{100}{10g}$
解之得:x=11.1g,y=11.7g.
(3)所得滤液即为NaCl溶液,溶液的总质量为100克,14g-11.1g是原混合物中的氯化钠的质量,而11.7g是新生成的,所以总质量为14g-11.1g+11.7g=14.6g.
所以滤液中溶质的质量分数=$\frac{14.6g}{100g}$×100%=14.6%
答:固体混合物中CaCl2的质量是11.1g,所得滤液中溶质的质量分数是14.6%.
故答案为:
(1)10g;(2)固体混合物中氯化钙的质量是11.1g;(3)所得滤液中溶质的质量分数是14.6%.
点评 本题主要考查学生运用化学方程式进行计算的能力.学生须认真分析题意,找出各物质间的关系,正确写出方程式,并能根据质量分数公式计算,才能正确解答.

| A. | H2SO4 AgNO3 NaCl | B. | CaCl2 K2CO3 NaNO3 | ||
| C. | CuSO4 NaCl KNO3 | D. | H2SO4 NaCl Na2SO4 |
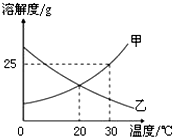 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.