题目内容
20.金属钛(Ti)硬度大、熔点高、耐腐蚀,被誉为“未来金属”.由钛铁矿(主要成分为FeTiO3)经过一系列反应制备钛和纳米TiO2的主要生产过程如下:(反应的部分生成物已略去)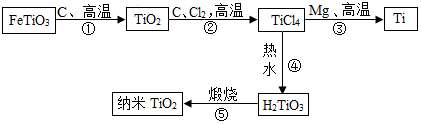
(1)FeTiO3叫钛酸亚铁,请标出钛酸亚铁中钛元素的化合价Fe$\stackrel{+4}{Ti}$O3.
(2)反应③属于置换反应,写出该反应的化学方程式:TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.
(3)生产过程中的反应可能是分解反应的是⑤(填序号).
(4)近年来,利用电解熔融TiO2生成氧气和钛的方法来制备金属钛获得成功.若电解80Kg的TiO2,理论上生成钛的质量是多少?(写出计算过程)
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
(1)FeTiO3叫钛酸亚铁,为亚铁,所以铁元素的化合价为+2价,而氧元素的化合价为-2价,设钛元素的化合价为x,根据化合物中化合价的代数和为零可得(+2)+x+(-2)×3=0,x=+4,标出钛酸亚铁中钛元素的化合价 Fe$\stackrel{+4}{Ti}$O3.
(2)反应③四氯化钛和镁反应,题目给出反应类型属于置换反应,所以生成物为钛和氯化镁,对应的化学方程式为:TiCl4+2Mg $\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.
(3)生产过程中的反应,只有⑤反应物为一种,所以⑤可能是分解反应
(4)解:设生成钛的质量为x
TiO2$\frac{\underline{\;通电\;}}{\;}$Ti+O2↑
80 48
80kg X
$\frac{80}{48}$=$\frac{80kg}{x}$
x=48kg
答:钛的质量为48k
故答案为:
(1)Fe$\stackrel{+4}{Ti}$O3.(只写化学式或化合价不得分)
(2)TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2.
(3)⑤.
(4)48kg.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
10.下列客观事实的微观解释正确的是( )
| 选项 | 客观事实 | 微观解释 |
| A | 水和过氧化氢的化学性质不同 | 分子构成不同,化学性质不同 |
| B | 盐酸能使紫色石蕊溶液变红 | 盐酸溶液中的Cl-使紫色石蕊溶液变红 |
| C | 轮胎在阳光下暴晒易爆裂 | 温度升高,分子的运动速率加快 |
| D | 氧化汞受热分解生成汞和氧气 | 构成氧化汞分子的汞原子和氧原子的间隔受热时增大 |
| A. | A | B. | B | C. | C | D. | D |
8.“类推”是化学学习过程中常用的思维方法.现有以下类推结果,其中正确的是( )
| A. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| B. | 因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 | |
| C. | 金属铝与盐酸反应生产AlCl3和H2,所以金属铁与盐酸反应生产FeCl3和H2 | |
| D. | 点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度 |
15.某花圃所种的花卉缺乏氮元素和钾元素,如果只施用一种化肥,则应施用( )
| A. | 硝酸钾 | B. | 碳酸钾 | C. | 尿素 | D. | 磷酸二氢钾 |
9.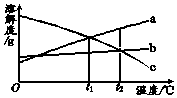 a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
 a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )
a、b、c三种物质的溶解度曲线如图所示.取等质量t1℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t1℃.下列说法不正确的是( )| A. | 原饱和溶液中,溶质的质量分数a=c>b | |
| B. | 恢复至t1℃时,析出溶质的质量a=c>b | |
| C. | 恢复至t1℃时,三种溶液都是饱和溶液 | |
| D. | 若继续升温至t2℃,三种溶液都是饱和溶液 |
 氧气用途广泛.
氧气用途广泛.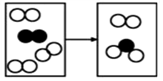
 B.
B. C.
C.
 2017年5月5日,中国首架无人机C919客机在浦东机场首飞成功.回答下列问题:
2017年5月5日,中国首架无人机C919客机在浦东机场首飞成功.回答下列问题: