题目内容
7.某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.这一现象激发起同学们的探究欲望,生成的是什么气体?【提出猜想】从物质组成元素的角度,放出的气体可能是SO2、O2、H2中的一种或几种.
【查阅资料】SO2易溶于水,它能与NaOH反应,生成Na2SO3和H2O.
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,若要检验可以用带火星的木条;
(2)乙同学认为是SO2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量.写出SO2与NaOH反应的化学方程式2NaOH+SO2=Na2SO3+H2O;
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体.
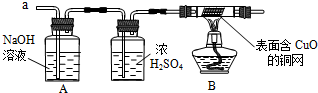
如果放出的气体是H2,在B中玻璃管内可观察到的现象是黑色铜网变红,有水珠出现,引起该现象的反应方程式为H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;丙同学认为:为确保安全,实验前应先验纯,方可采用上面的装置进行实验.
分析 铁是一种活动性较强的金属,可以与酸反应产生氢气,产生的氢气具有可燃性和还原性,若不纯点燃或加热易爆炸,可以用来还原某些金属氧化物,铁还可以与硫酸铜溶液反应,置换出其中的铜;氧气能使带火星的木条复燃;二氧化硫是酸性气体,能与碱反应生成盐和水.
解答 解:(1)氧气具有助燃性,更是带火星的木条复燃,所以本题答案为:用带火星的木条试验,看木条是否复燃;
(2)二氧化硫是酸性气体,可以与碱氢氧化钠反应生成亚硫酸钠和水,故本题答案为:SO2+2NaOH=Na2SO3+H2O,
(3)氢气具有可燃性,氢气可以将氧化铜被还原为铜同时生成水,所以黑色铜网变红,有水珠出现;化学方程式为:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
如若不纯,点燃或加热时易产生爆炸事故,所以使用前要注意验纯,一般采用小试管收集点燃的方法,不纯时能发出尖锐的爆鸣声,故本题答案为:实验时剩余气体B通过加热的试管易发生爆炸事故,堵住试管囗,靠近火焰点火,尖锐的爆鸣声;
无答案为:(1)带火星的木条
(2)2NaOH+SO2=Na2SO3+H2O
(3)黑色铜网变红,有水珠出现;H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;验纯.
点评 本题综合考查了金属的化学性质、氧气的检验、使用氢气的注意事项以及碱的部分性质,常见气体的鉴别主要有氧气、二氧化碳、氮气、氢气、空气等,选择鉴别方法时,要根据气体性质的差异.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
17.2015年某电视台举办的“3•15”晚会,曝出某品牌金饰品掺假的事件,引起同学们的好奇,某化学兴趣小组在老师的帮助下,对几种常见金属饰品所含的金属进行了相关的探究活动.
【提出问题】(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
【查阅资料】(1)假黄金通常是黄铜(Cu-Zn合金);
(2)钯(Pd)呈银白色,有金属光泽,可用作饰品.
【实验药品】钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】(1)鉴别黄金样品的真、假,取黄金样品于试管中,滴加稀盐酸后,观察到黄金样品表面有气泡产生,该气体是氢气,说明此样品为假(选填“真”或“假”)黄金.
(2)探究钯的金属活动性.依据生活经验,同学们猜想钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
初步得出结论:钯、银、铂的金属活动性由强到弱的顺序为银>钯>铂.
【废液处理】
(3)转化成沉淀.小组同学将所有液体倒入废液缸中,出现白色沉淀.写出产生该现象的化学方程式HCl+AgNO3═AgCl↓+HNO3.(写出一个即可).
【提出问题】(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
【查阅资料】(1)假黄金通常是黄铜(Cu-Zn合金);
(2)钯(Pd)呈银白色,有金属光泽,可用作饰品.
【实验药品】钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】(1)鉴别黄金样品的真、假,取黄金样品于试管中,滴加稀盐酸后,观察到黄金样品表面有气泡产生,该气体是氢气,说明此样品为假(选填“真”或“假”)黄金.
(2)探究钯的金属活动性.依据生活经验,同学们猜想钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 把钯浸入硝酸银溶液中 | 无明显现象 | 钯的活动性比银弱 |
| 把铂浸入氯化钯溶液中 | 无明显现象 | 钯的活动性比铂强 |
【废液处理】
(3)转化成沉淀.小组同学将所有液体倒入废液缸中,出现白色沉淀.写出产生该现象的化学方程式HCl+AgNO3═AgCl↓+HNO3.(写出一个即可).
18.下列说法正确的是( )
| A. | 煤、石油、乙醇是三种重要的化石燃料 | |
| B. | 全力开采化石燃料用于居民供暖 | |
| C. | 图书档案着火宜用水基型灭火器扑灭 | |
| D. | 室内着火时不要急于打开门窗 |
15.下列处理方法恰当的是( )
| A. | 酒精灯的酒精碰洒在桌上燃烧起来,用湿抹布盖灭 | |
| B. | 厨房天然气泄漏,立即打开排风扇通风 | |
| C. | 图书档案起火,用大量水浇灭 | |
| D. | 室内放一盆水,以防煤气(含CO)中毒 |
2.下列物质的鉴别,所选择的试剂或方法错误的是( )
| 选项 | 需区别的物质 | 选择的试剂或方法 |
| A | 食醋与酒精 | 闻气味 |
| B | 空气与氧气 | 带火星的木条 |
| C | 二氧化锰和活性炭 | 看颜色 |
| D | 一氧化碳与二氧化碳 | 燃着的木条 |
| A. | A | B. | B | C. | C | D. | D |
16.取三种植物的花瓣分别放在研钵中,加入酒精研磨,得到花汁.各取少许花汁,用稀酸和稀碱进行检验,结果如下表所示:则下列说法中正确的是( )
| 花的种类 | 花汁在酒精中的颜色 | 花汁在酸溶液中的颜色 | 花汁在碱溶液中的颜色 |
| 玫瑰 | 粉红色 | 粉红色 | 绿色 |
| 万寿菊 | 黄色 | 黄色 | 黄色 |
| 雏菊 | 无色 | 无色 | 黄色 |
| A. | 研磨花瓣过程中加入酒精是为了溶解其中的色素 | |
| B. | 可用雏菊花汁来区别H2SO4和K2SO4溶液 | |
| C. | 25℃时,遇到pH=10的溶液,玫瑰花汁会变成粉红色 | |
| D. | 上述三种花汁都能用作酸碱指示剂 |
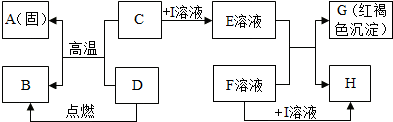
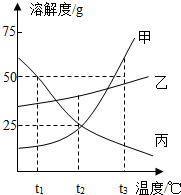 如图是甲、乙、丙三种物质的溶解度曲线.
如图是甲、乙、丙三种物质的溶解度曲线.