题目内容
某工厂排出的废水中含有Na2CO3,为测得其含量化学兴趣小组取该废水100g,向其中加入19.2g稀盐酸,恰好完全反应(其他杂质不与盐酸反应,气体全部逸出)得到117g溶液。试计算:
(1)反应后生成CO2的质量为 g。
(2)原废水中Na2CO3的质量分数;反应后所得溶液的质量分数。(请写出计算过程)
解:(1)反应生成CO2气体的质量为:100g+19.2g﹣117g=2.2g,(1分)
(2)设生成氯化钠的质量为x,原废水中Na2CO3的质量为y
Na2CO3+2HC1═2NaC1+H2O+CO2↑,(1分)
106 117 44
y x 2.2g
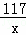 =
=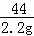 , 106:y=44:2.2
, 106:y=44:2.2
x=5.85g,(1分)  y=5.3 g(1分)
y=5.3 g(1分)
反应后所得溶液中溶质的质量分数为: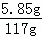 ×100%=5%,(1分)
×100%=5%,(1分)
废水中Na2CO3的质量分数为(5.3 g∕100 g)*100%=5.3%(1分)
答:反应后所得溶液中溶质的质量分数为5%;原废水中Na2CO3的质量分数为5.3%。

 出彩同步大试卷系列答案
出彩同步大试卷系列答案通过下列实验操作和现象能得出相应结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向一瓶空气样品和一瓶呼出气体的样品中各滴入相同滴数的澄清石灰水,振荡 | 空气样品的瓶中无明显变化,呼出气体的瓶中石灰水变浑浊 | 空气中不含CO2,呼出气体中含有CO2 |
| B | 在试管中加入氢氧化钠固体,再加入一定量的水,振荡,用手触摸试管外壁 | 手感觉热 | 物质溶解时都伴随放热现象 |
| C | 用拇指堵住集满氢气的试管口,靠近火焰移开拇指点火 | 听到尖锐的爆鸣声 | 氢气不纯 |
| D | 将燃着的木条伸入一瓶未知气体中 | 木条熄灭 | 该气体一定是CO2 |
在反应4Zn+10HNO3═4Zn(NO3)2 +X+3H2O中,X的化学式为( )
+X+3H2O中,X的化学式为( )
|
| A. | NH3 | B. | NH4NO3 | C. | NO | D. | NO2 |

 出B组任一试管中发生反应的化学方程式: 。
出B组任一试管中发生反应的化学方程式: 。
 ”聚集成的物质 (填“可能”或“不可能”)是氧化物,参加反应的两种反应物的分子个数比为 。
”聚集成的物质 (填“可能”或“不可能”)是氧化物,参加反应的两种反应物的分子个数比为 。 不怕巷子深”,说明了分子在不断运动
不怕巷子深”,说明了分子在不断运动 去二氧化碳中少量的一氧化碳:2CO+O2 点燃 2CO2
去二氧化碳中少量的一氧化碳:2CO+O2 点燃 2CO2