题目内容
13.根据下列实验装置图,回答有关问题:
(1)实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,选用C收集氧气时,证明氧气已收集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满.
(2)实验室用大理石和稀盐酸制取二氧化碳时,选用的发生装置为B(填字母),一般不选用E收集二氧化碳的原因是二氧化碳能溶于水,且能与水反应.
(3)实验室用稀硫酸和锌粒制取氢气的化学方程式为Zn+H2SO4═ZnSO4+H2↑,选用F收集氢气时,氢气应从b(填“a”或“b”)端进入.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.证明氧气已收集满的方法是:将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水且与水反应,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.
解答 解:(1)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;证明氧气已收集满的方法是:将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水且与水反应,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:B;二氧化碳能溶于水,且能与水反应;
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;选用F收集氢气时,氢气应从短管进入,因为氢气的密度比空气小,故答案为:Zn+H2SO4═ZnSO4+H2↑;b
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案| A. |  | B. |  | C. |  | D. |  |
| A. | 蛋白质、糖类都属于有机物 | B. | 误食重金属盐可喝鲜牛奶解毒 | ||
| C. | 钛合金、玻璃钢都属于复合材料 | D. | 油脂由C、H、O三种元素组成 |
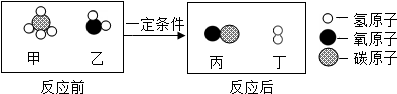
下列对该反应的叙述不正确的是( )
| A. | 反应前后原子个数不变 | |
| B. | 乙、丙都属于氧化物 | |
| C. | 生成的丙和丁的分子个数比为1:3 | |
| D. | 若将16g的甲和20g的乙混合反应,则生成丙和丁的质量之和一定为36g |
| A. | 氧气 | B. | 二氧化碳 | C. | 碳酸 | D. | 氩气 |
| A. |  徽州石雕 | B. |  芜湖铁画 | ||
| C. |  三河米酒 | D. |  阜阳剪纸 |